Bài viết được viết bởi ThS, BS. Mai Viễn Phương, Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Ung thư dạ dày (GC) đứng hàng thứ ba trong nguyên nhân chính gây tử vong do bệnh lý ác tính trên toàn thế giới, và nội soi dạ dày tá tràng (EGD) được coi là công cụ chẩn đoán tốt nhất cho ung thư ở giai đoạn đầu và trí tuệ nhân tạo đóng vai trò quan trọng trong việc điều trị ung thư dạ dày.
Trí tuệ nhân tạo (AI) dựa trên các yếu tố thông minh nhân tạo thực hiện các chức năng liên quan đến tâm trí con người, chẳng hạn như học tập và giải quyết vấn đề.
Trong nội soi, AI đã bắt đầu hỗ trợ cải thiện tỷ lệ phát hiện polyp đại tràng và phát hiện u tuyến (ADR), để phân biệt giữa các tổn thương lành tính và tiền ung thư dựa trên việc giải thích các mô hình bề mặt của chúng.
Học máy (ML) và học sâu (DL) có thể được coi là các lĩnh vực con của trí tuệ nhân tạo. ML là một dạng trí tuệ nhân tạo có thể hỗ trợ quá trình ra quyết định, cho phép cải tiến các thuật toán được áp dụng mà không cần lập trình, bao gồm cả kiểm tra dữ liệu và triển khai các mô hình mô tả và dự đoán (Hình 1).
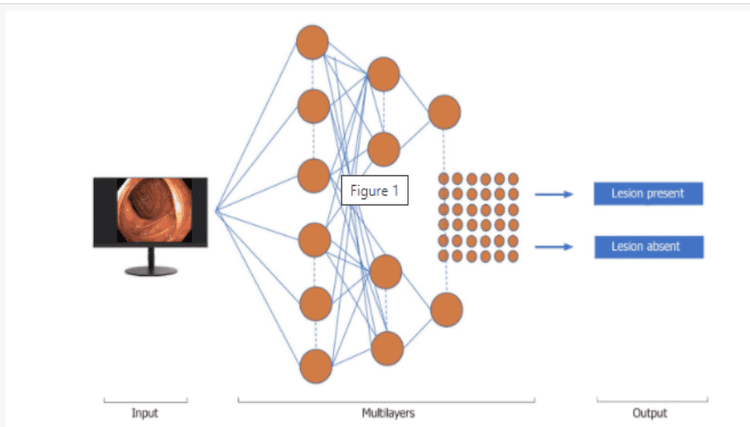
Thuật toán học máy (Machine learning – ML) được phân biệt thành các phương pháp có giám sát và không được giám sát. Một ví dụ của công nghệ học máy được giám sát, mạng nơ-ron nhân tạo (ANN), phản ánh chức năng sơ đồ của não. Mỗi nơron là một đơn vị tính toán và tất cả các nơron được kết nối để tạo ra một mạng. Các thuật toán học máy và mạng nơ-ron phức tạp (CNN) đã được tạo ra để huấn luyện phần mềm phân biệt vùng bình thường với vùng bất thường trong lòng ruột. Để phát hiện polyp, công nghệ học máy sử dụng một số đặc điểm cố định, chẳng hạn như kích thước, hình dạng và các kiểu niêm mạc của polyp.
1. Trí tuệ nhân tạo và ung thư dạ dày
Ung thư dạ dày (GC) đứng hàng thứ ba trong nguyên nhân chính gây tử vong do bệnh lý ác tính trên toàn thế giới, và nội soi dạ dày tá tràng (EGD) được coi là công cụ chẩn đoán tốt nhất cho ung thư ở giai đoạn đầu. Việc điều trị u dạ dày phụ thuộc vào độ sâu của sự xâm lấn dưới niêm mạc; thực sự, đối với các khối u trong niêm mạc đã biệt hóa (M) hoặc những khối u xâm lấn vào lớp dưới niêm mạc nông (≤ 500 lm: SM1), kỹ thuật cắt niêm mạc EMR hoặc cắt bóc tách dưới niêm mạc ESD được thực hiện để cắt bỏ tổn thương, trong khi những khối u có xâm lấn sâu dưới niêm mạc (> 500 lm: SM2) nên được điều trị bằng phẫu thuật để tránh nguy cơ tiềm ẩn xâm lấn và di căn tại chỗ. Nội soi phóng đại kết hợp với NBI hoặc FICE (tăng cường màu sắc linh hoạt của hình ảnh quang phổ) hữu ích về mặt lâm sàng trong việc phân biệt ác tính dạ dày với các vùng không ác tính. Tuy nhiên, chẩn đoán quang học này hoàn toàn phụ thuộc vào chuyên môn và kinh nghiệm của người thực hiện, điều này ngăn cản việc sử dụng chung trong thực hành lâm sàng.
2. Kết quả một số nghiên cứu
Hai nghiên cứu ngẫu nhiên đa trung tâm đã kiểm tra hiệu suất của nội soi có / không có sự hỗ trợ của các thuật toán AI. Nghiên cứu đầu tiên ước tính hiệu suất của hệ thống DL thời gian thực, WISENSE, để kiểm soát sự hiện diện của các điểm mù trong nội soi tiêu hoá trên. Nhìn chung, 324 bệnh nhân thực hiện nội soi ngẫu nhiên có hoặc không sử dụng hệ thống WISENSE theo dõi các điểm mù với độ chính xác trung bình 90% và độ chính xác riêng biệt cho từng vị trí dao động 70,2% -100% trong 107 video nội soi trực tiếp.
Độ nhạy và độ đặc hiệu trung bình là 87,6% và 95%, tương ứng nằm trong khoảng 63,4% -100% và 75% -100%. Đối với quy trình nội soi thời gian, hệ thống WISENSE dự đoán chính xác thời gian bắt đầu và kết thúc trong video lần lượt là 93,5% (100/107) và 97,2% (104/107) .
Miyaki và cộng sự, đã phát triển phần mềm cho phép đánh giá định lượng GC niêm mạc trên hình ảnh nội soi tiêu hóa phóng đại thu được bằng FICE. Họ đã thông qua một bộ khung đặc điểm có các bộ mô tả biến đổi tính năng bất biến ở quy mô được lấy mẫu dày đặc để phóng đại hình ảnh FICE của 46 trường hợp ung thư dạ dày trong niêm mạc sau đó so sánh với các phát hiện mô học. Hệ thống CAD cho phép độ chính xác phát hiện là 86%, độ nhạy và độ đặc hiệu là 85% và 87% đối với chẩn đoán ung thư.
Trong nghiên cứu của Kanesaka và cộng sự, tổng số 127 bệnh nhân có nội soi dạ dày đóng góp vào 127 hình ảnh M-NBI ung thư, trong khi 20 bệnh nhân không có nội soi dạ dày cung cấp cho 60 hình ảnh M-NBI không ung thư. Các tác giả đã tạo ra phần mềm cho phép xác định cả ung thư dạ dày và vạch ra ranh giới giữa các vùng ác tính và không ác tính. Thuật toán CAD này được thiết kế để khảo sát các đặc điểm ma trận đồng xuất hiện mức xám của các lát pixel được phân vùng của hình ảnh NBI phóng đại và một máy vectơ hỗ trợ đã được sử dụng cho phương pháp học máy. Các mô hình cho thấy độ nhạy 97% và độ đặc hiệu 95% trong việc phân biệt ung thư, trong khi hiệu suất đối với sự phù hợp vùng hiển thị độ nhạy và độ đặc hiệu, tương ứng là 81% và 66%.
3. Ứng dụng của mạng nơ-ron phức tạp CNN trong đánh giá ung thư dạ dày
Vào năm 2018, Hirasawa và cộng sự , đã phát triển một hệ thống chẩn đoán dựa trên AI để phát hiện ung thư dạ dày, sử dụng CNN mô phỏng não người.
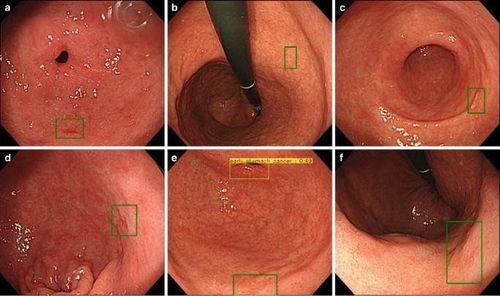
Tổng số 714 trong số 2.296 bộ hình ảnh xét nghiệm (31,1%) xác nhận sự hiện diện của ung thư dạ dày, và 84,1% bị teo dạ dày mức độ trung bình / nặng. CNN đã sử dụng 47 giây để phân tích 2.296 hình ảnh xét nghiệm, chẩn đoán tổng thể 232 bệnh nhân ung thư dạ dày, 161 tổn thương không ác tính, 71 trong số 77 là tổn thương ung thư dạ dày với độ nhạy 92,2%. Phần lớn các tổn thương dạ dày (98,6%) có đường kính ≥ 6 mm được CNN xác định chính xác, ngoài ra đối với tất cả các ung thư biểu mô xâm lấn (T1b hoặc sâu hơn). Các tổn thương không được chẩn đoán có bề mặt lõm xuống và thường là ung thư nội mạc với mô phân biệt, mà việc phân biệt với viêm dạ dày cũng là một thách thức đối với các bác sĩ nội soi có kinh nghiệm. Một lý do thông thường khác cho việc chẩn đoán sai là các vị trí giải phẫu của cơ tim, mạch môn vị và môn vị.
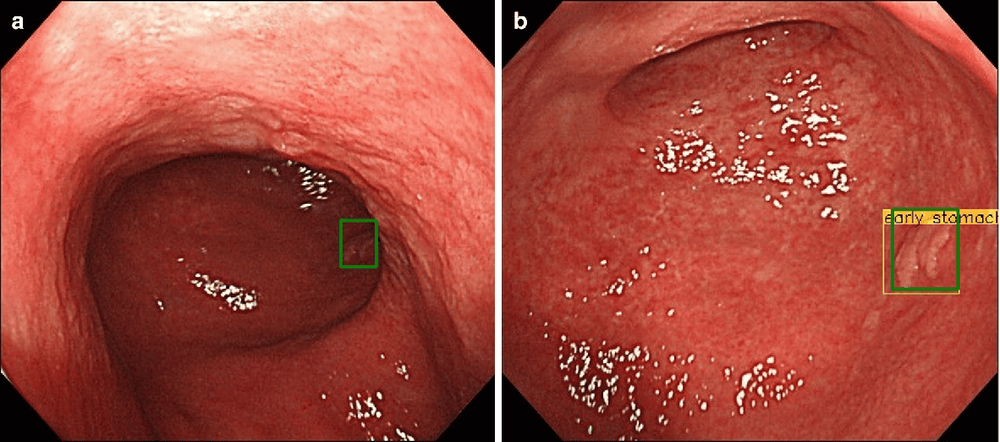
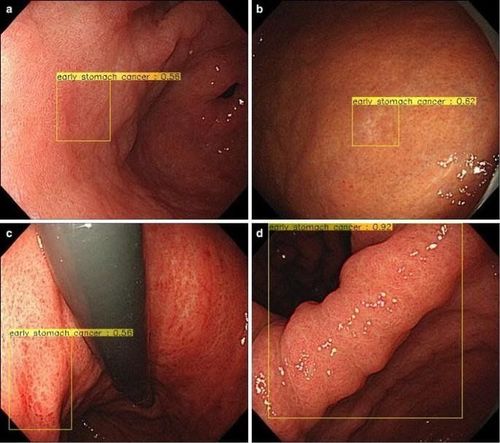
Zhu và cộng sự đã xem xét tiềm năng của AI để giải quyết dự đoán về độ sâu xâm lấn của GC sơ khai. Đặc biệt, họ đã phát triển và xác thực mô hình AI CNN-CAD sử dụng thuật toán học sâu để xác định độ sâu xâm lấn của ung thư dạ dày (“M / SM1” so với “SM2 hoặc sâu hơn”).
Tổng cộng có 790 hình ảnh nội soi của ung thư dạ dày được sử dụng cho thuật toán học máy, trong khi 203 hình ảnh bổ sung, hoàn toàn tự trị từ tài liệu học tập, được xử lý như một bộ thử nghiệm. Mô hình AI cho thấy độ nhạy và độ đặc hiệu là 76% và 96%, tương ứng trong việc phân biệt SM2 hoặc sự xâm lấn sâu hơn của ung thư, với hiệu suất chẩn đoán cao hơn so với mô hình mà các nhà nội soi đạt được. Độ đặc hiệu cao này có thể làm giảm sự đánh giá quá mức về xâm lấn khối u, điều này sẽ góp phần gián tiếp làm giảm các phẫu thuật có thể tránh được đối với khối u ác tính M / SM1. Hơn nữa, trong nghiên cứu này, hệ thống CNN-CAD cũng đạt được độ chính xác và độ đặc hiệu cao hơn đáng kể so với cả bác sĩ nội soi được đào tạo chuyên nghiệp và cơ sở.
4. Vai trò của AI trong dự đoán tiên lượng của bệnh nhân mắc ung thư dạ dày
AI có thể hỗ trợ các bác sĩ dự đoán tiên lượng của bệnh nhân mắc ung thư dạ dày. Một số thử nghiệm lâm sàng quan trọng đánh giá các chiến lược bổ trợ của ung thư dạ dày tiến triển cao đã được sản xuất trong thập kỷ qua, nhưng liệu pháp phù hợp nhất cho ung thư dạ dày cho đến nay vẫn chưa chắc chắn. Bên cạnh đó, hai nghiên cứu cảnh quan phân tử đương đại đã chứng minh sự hiện diện của các phân nhóm ung thư dạ dày phân tử khác nhau. Một mô hình dựa trên thuật toán học sâu (mạng tái phát sinh tồn, SRN) được phát triển để dự đoán các biến cố sống sót cho tổng số 1190 bệnh nhân ung thư dạ dày, dựa trên dữ liệu lâm sàng / bệnh lý cũng như phác đồ điều trị, dự đoán kết quả tại từng thời điểm trong thời gian 5 thời gian giám sát năm. SRN chỉ ra rằng loại phụ trung mô của ung thư dạ dày nên kích thích một chiến lược điều trị sau phẫu thuật phù hợp do hậu quả của tỷ lệ tái phát rất lớn. Ngược lại, SRN quan sát thấy rằng các ung thư dạ dày không ổn định tế bào vi mô và dạng u nhú cho thấy tiên lượng thuận lợi hơn đáng kể sau khi hóa trị bao gồm capecitabine và cisplatin. SRN đạt tỷ lệ sống sót là 92%, 5 năm sau khi phẫu thuật cắt bỏ cắt dạ dày. Mô hình ANN được sử dụng để đánh giá 452 bệnh nhân ung thư dạ dày, xác định thời gian sống sót với độ chính xác khoảng 90%, và tập trung vào việc tạo ra một cấu trúc ANN phù hợp với khả năng xử lý dữ liệu được kiểm duyệt. Cụ thể, 5 bộ mô hình ANN chuyển tiếp điểm thời gian duy nhất đã được tạo ra để dự đoán kết quả của bệnh nhân ung thư dạ dày trong các khoảng thời gian đều đặn (hàng năm) cho đến năm thứ năm sau khi cắt dạ dày. Do đó, các mô hình dự đoán ANN thể hiện độ chính xác, độ nhạy và độ đặc hiệu, lần lượt là 88,7% -90,2%, 70,2%-92,5% và 66,7%-96,2%.
5. Một số hạn chế của trí tuệ nhân tạo
Trí tuệ nhân tạo AI có thể đại diện cho một phương pháp chẩn đoán cần thiết cho các bác sĩ nội soi và bác sĩ tiêu hóa để điều trị bệnh nhân phù hợp và dự đoán kết quả lâm sàng của họ. Trí tuệ nhân tạo dường như đặc biệt có giá trị trong nội soi tiêu hóa, để cải thiện việc phát hiện các tổn thương tiền ác tính và ác tính, hoặc tổn thương viêm, xuất huyết tiêu hóa và các bệnh lý tuyến tụy. Tuy nhiên, những hạn chế hiện tại của Trí tuệ nhân tạo bao gồm thiếu bộ dữ liệu chất lượng cao để phát triển thuật toán học máy ML . Hơn nữa, một bằng chứng quan trọng được sử dụng để xây dựng các thuật toán thuật toán học máy chỉ đến từ các nghiên cứu tiền lâm sàng. Chắc chắn, cũng cần phải thừa nhận các vấn đề đạo đức vì AI không nhận thức được các lựa chọn hoặc trách nhiệm pháp lý của bệnh nhân. Các vấn đề về quyền riêng tư có thể được giải quyết bằng cách sử dụng các bộ dữ liệu được liên kết không liên quan đến các máy chủ tập trung. Các nghiên cứu ngẫu nhiên trong tương lai có thể trực tiếp làm tăng giá trị tổng thể (chất lượng so với chi phí) của CNN bằng cách kiểm tra tác động của nó đối với nội soi đại tràng giám sát, thời gian nội soi, polyp và ADR, và chi phí bệnh lý. Vì khoa học AI đang trong quá trình phát triển, những hạn chế hiện tại phải được coi là thách thức trong tương lai, vì vậy chúng thực sự được kế thừa trong các ứng dụng y học, bao gồm khả năng dự đoán khó đối với các tình huống có đặc điểm là không chắc chắn. Nhìn chung, AI đang cách mạng hóa công nghệ và tác động đến các khía cạnh đạo đức khác như thay thế công việc của con người bằng máy móc, nhưng đây luôn là một câu hỏi mở kể từ cuộc cách mạng công nghiệp. Điều có thể làm là thúc đẩy sự hợp tác lẫn nhau thông qua các ứng dụng nội soi tiêu hóa, để cùng hưởng lợi từ những thành tựu trong cả hai lĩnh vực khoa học.
Ung thư dạ dày là căn bệnh nguy hiểm, phổ biến tại Việt Nam và đe dọa đến tính mạng của người bệnh rất lớn. Để phòng tránh và phát hiện sớm ung thư dạ dày, bạn nên điều trị viêm loét dạ dày sớm và thường xuyên tầm soát ung thư dạ dày để chủ động phát hiện nguy cơ mắc bệnh sớm từ giai đoạn đầu, mang lại kết quả điều trị tốt nhất.
Xem thêm: Hướng dẫn chẩn đoán ung thư dạ dày
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo
1. Russell S, Norvig P. Artificial Intelligence: A Modern Approach, Global Edition. 3rd editon. London: Pearson, 2016.
2. Colom R, Karama S, Jung RE, Haier RJ. Human intelligence and brain networks. Dialogues Clin Neurosci. 2010;12:489-501. [PubMed]
3. Pohl H, Welch HG. The role of overdiagnosis and reclassification in the marked increase of esophageal adenocarcinoma incidence. J Natl Cancer Inst. 2005;97:142-146. [PubMed] [DOI]
4. Gaetano Cristian Morreale, Emanuele Sinagra, và cộng sự, Emerging artificial intelligence applications in gastroenterology: A review of the literature, Artif Intell Gastrointest Endosc. Jul 28, 2020; 1(1): 6-18