Cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu đã và đang được nghiên cứu bởi các chuyên gia trong khoảng 100 năm trở lại đây. Đây là một bệnh lý viêm ruột mãn tính, tác động đến đại tràng và có cơ chế bệnh sinh chưa quá rõ ràng trong quá khứ. Tuy nhiên, trong một thế kỷ qua, những ghi nhận về bệnh lý đặc trưng đã dần được hoàn thiện.
Bài viết này được viết dưới sự hướng dẫn chuyên môn của bác sĩ Thạc sĩ, Bác sĩ Mai Viễn Phương, Bác sĩ nội soi tiêu hóa, tại Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
1. Tổng quan về cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu
Theo sự đồng thuận của Tổ chức Crohn và Viêm đại tràng (ECCO) năm 2017, viêm loét đại trực tràng chảy máu được định nghĩa là bệnh lý viêm mạn tính, đặc trưng bởi tình trạng viêm niêm mạc đại tràng liên tục và tổn thương u hạt trên mô bệnh học. Bệnh tác động đến trực tràng và đại tràng với các mức độ khác nhau, trải qua từng đợt tiến triển và lui bệnh.
Hiện tại, cơ chế bệnh sinh của bệnh lý này vẫn chưa được làm rõ hoàn toàn. Tuy nhiên, giả thuyết phổ biến cho rằng tình trạng này là kết quả của sự phối hợp bởi nhiều yếu tố, bao gồm di truyền, môi trường và hệ vi sinh đường ruột. Qua đó, bệnh lý này dẫn đến tình trạng đáp ứng viêm không phù hợp. Một số cơ chế gây bệnh đã được xác định bao gồm:
- Rối loạn hệ vi khuẩn đường ruột: Sự suy giảm các chủng vi khuẩn có lợi (đặc biệt là Firmicutes và Bacteroidetes) dẫn đến sự xâm nhập qua lớp nhầy của vi khuẩn có hại.
- Tăng bộc lộ thụ thể giống Toll (TLR-4).
- Tích lũy tiền chất glycosyl hóa của mucin: Gây giảm chất lượng chất nhầy ruột, làm suy yếu hàng rào bảo vệ.
- Kích hoạt tế bào miễn dịch gây bệnh: Tế bào đuôi gai mang kháng nguyên CD10 giải phóng ra TL27, kích hoạt các tế bào T CD4 và tế bào diệt tự nhiên chưa trưởng thành biệt hóa. Sau đó, tế bào T CD4 biệt hoá thành tế bào lympho T điều hoà và lympho T hỗ trợ rồi tiếp tục sản xuất ra các chất hoạt hóa bạch cầu ái toan. Tế bào diệt tự nhiên được hoạt hóa sản xuất ra IL-13 có tác dụng phá hủy tế bào biểu mô, biến đổi chức năng vùng nối giữa các tế bào, gây xơ hóa và IL-23 có tác dụng hoạt hóa tế bào Th7 sản xuất IL17 từ đó gây hóa ứng động bạch cầu trung tính.
- Sự hoạt hoá tế bào lympho B được sản xuất từ các kháng thể trong cơ thể.
Mặc dù sự liên quan giữa yếu tố di truyền và sự khởi phát, tiến triển của bệnh này không được chứng minh rõ ràng như trong bệnh Crohn, các nghiên cứu trên trẻ sinh đôi cho thấy tỷ lệ mắc bệnh này ở trẻ sinh đôi cùng trứng là 16%, trong khi tỷ lệ ở các cặp sinh đôi khác trứng là 2%.
Hiện nay, các chuyên gia đã xác định được 47 vị trí gen liên quan đến viêm loét đại trực tràng chảy máu, trong đó 20 vị trí trùng lặp với bệnh Crohn ( ví dụ như IL-10, IL-23 hay các con đường liên quan tới Janus-kinase, v.v.).
Một số gen đặc hiệu cho căn bệnh này bao gồm yếu tố nhân tế bào gan (như hepatocyte nuclear factor-4a, cadherin 1 và laminin-B1). Đây là các gen có vai trò huy động bạch cầu, từ đó làm suy yếu hàng rào bảo vệ của tế bào.
2. Vai trò của hệ vi khuẩn đường ruột trong viêm loét đại trực tràng chảy máu
Hệ vi khuẩn đường ruột được hình thành hoàn chỉnh trong vài tháng đầu sau sinh và duy trì khá ổn định trong suốt cuộc đời, mặc dù có thể thay đổi ít nhiều tùy theo hoàn cảnh. Hệ vi khuẩn này bao gồm khoảng 15.000 - 36.000 chủng khác nhau, trong đó các nhóm chủ yếu là Firmicutes và Bacteroidetes.

Trong điều kiện sinh lý bình thường, hệ vi khuẩn đường ruột đóng vai trò quan trọng trong sự trưởng thành của tế bào niêm mạc ruột, duy trì cân bằng, cung cấp dinh dưỡng, bảo vệ và sửa chữa tổn thương niêm mạc.
Trong các bệnh lý viêm ruột, nhiều nghiên cứu cho thấy số lượng vi khuẩn tại niêm mạc ruột tăng cao hơn ở người khỏe mạnh, nhưng tính đa dạng của chúng lại giảm từ 30 - 50%. Sự thay đổi này càng khác biệt hơn giữa bệnh Crohn và viêm loét đại trực tràng chảy máu.
Trong trường hợp này, những chủng vi khuẩn có lợi như Bacteroidetes và Firmicutes (đặc biệt là Eubacterium và Lactobacillus) giảm đáng kể, trong khi các vi khuẩn gây hại (chẳng hạn như E. coli) lại tăng lên. Mặc dù các thay đổi này đóng vai trò quan trọng trong cơ chế sinh bệnh của viêm ruột nhưng vẫn còn những tranh cãi về việc liệu chúng là nguyên nhân hay hậu quả của quá trình viêm niêm mạc.
Một nghiên cứu đã so sánh hệ vi khuẩn tại vùng niêm mạc tổn thương và vùng niêm mạc lành ở bệnh nhân viêm loét đại trực tràng có chảy máu đang trong giai đoạn hoạt động của bệnh. Kết quả cho thấy không có sự khác biệt đáng kể về hệ vi khuẩn giữa hai vùng này.
Điều này gợi ý rằng, sự thay đổi hệ vi khuẩn đường ruột có thể là yếu tố nguyên phát, đóng vai trò quan trọng trong cơ chế bệnh sinh của bệnh viêm loét đại trực tràng xuất huyết hơn là hậu quả của quá trình viêm.
3. Hàng rào bảo vệ ruột và sự liên quan đến cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu
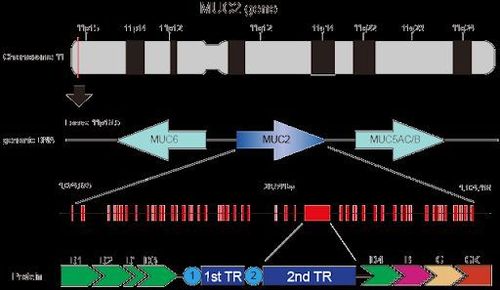
Niêm mạc ruột được bao phủ bởi lớp chất nhầy có vai trò bảo vệ, ngăn chặn sự tiếp xúc trực tiếp của các yếu tố gây bệnh với lớp biểu mô bên dưới. Lớp chất nhầy này bao gồm các thành phần protein, carbohydrate, lipid, trong đó glycoprotein mucin (mã hóa bởi gen MUC2) là thành phần chính.
Chất nhầy được tổng hợp trong lưới nội bào của tế bào đài và tế bào Paneth, trải qua quá trình glycosyl hóa ở hệ Golgi, tiếp đến là sulfat hóa và được giải phóng ra ngoài dưới dạng các hạt chứa phức hợp chất nhầy.
Ngoài ra, chất nhầy còn chứa nhiều yếu tố chống vi khuẩn như defensin, cathelicidin và lysozyme được sản xuất từ tế bào Paneth và tế bào ruột, cùng với đó là trefoil peptide, được tiết ra cùng MUC2 từ tế bào đài.
Ở người bệnh bị viêm loét đại trực tràng xuất huyết giai đoạn hoạt động, lớp chất nhầy bảo vệ niêm mạc ruột có nhiều thay đổi đáng kể. Cụ thể những sự thay đổi này bao gồm:
- Giảm bề dày của lớp chất nhầy.
- Giảm số lượng tế bào đài.
- Tăng sự thâm nhập của tế bào bạch cầu trung tính.
- Sự tiếp xúc một cách trực tiếp của vi khuẩn đường ruột với lớp dưới niêm mạc.
Khi hàng rào bảo vệ này bị tổn thương, tính thẩm thấu của màng tế bào biểu mô thay đổi, làm ảnh hưởng đến vùng nối giữa các tế bào. Điều này khiến các kháng nguyên vi khuẩn dễ dàng tiếp xúc với hệ miễn dịch, qua đó kích hoạt các phản ứng từ cả miễn dịch bẩm sinh và miễn dịch mắc phải, góp phần vào cơ chế sinh bệnh.
4. Các tế bào có liên quan đến cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu
Những tế bào hiện đã được xác định có liên quan tới cơ chế sinh bệnh của căn bệnh này gồm:
4.1 Tế bào trình diện kháng nguyên
Trình diện kháng nguyên cho các tế bào miễn dịch ở ruột là bước đầu tiên trong việc kích hoạt các cytokine viêm. Tế bào đuôi gai có các thụ thể nhận diện mẫu (PRR - pattern-recognition receptor) sẽ sở hữu khả năng phản ứng với các kháng nguyên nội và ngoại bào. Khi hàng rào biểu mô mất tính toàn vẹn, kháng nguyên có thể xâm nhập vào lớp màng liên kết, kích hoạt các tế bào đuôi gai.
Lipopolysaccharide của vi sinh vật là một yếu tố quan trọng thúc đẩy sự trưởng thành của tế bào đuôi gai. Sau khi được hoạt hóa, tế bào đuôi gai giải phóng IL-12, góp phần vào quá trình trưởng thành của tế bào T ban đầu, đồng thời tạo ra các cytokine và chemokine viêm, thu hút bạch cầu trung tính và kích hoạt các tế bào miễn dịch khác.
Đại thực bào nằm trong niêm mạc đường tiêu hóa cũng được kích hoạt khi có sự xuất hiện của kháng nguyên. Quá trình này dẫn đến sự giải phóng các yếu tố tiền viêm, bao gồm TNF-4, IL-1, IL-6, IL-8, IL-12, IL-18 và IL-23.
Bên cạnh đó, đại thực bào còn sản xuất các chất chuyển hóa dạng hoạt động của oxy và nitơ, các protease có khả năng giáng hoá hệ cấu trúc ngoại bào. Do đó, vai trò của đại thực bào không chỉ dừng lại ở việc thúc đẩy tình trạng viêm mà còn rất quan trọng trong giai đoạn phục hồi, khi các tổn thương niêm mạc ruột bắt đầu lành lại.
4.2 Tế bào lympho T hỗ trợ
Cơ chế bệnh sinh liên quan đến hệ miễn dịch mắc phải trong viêm loét đại trực tràng xuất huyết bắt đầu từ quá trình trình diện kháng nguyên của tế bào đuôi gai, dẫn đến việc giải phóng các cytokine có vai trò kích hoạt và biệt hóa tế bào T.
Tế bào T có thể biệt hóa thành tế bào T điều hòa hoặc tế bào T hoạt động. Sự mất cân bằng giữa các dòng tế bào T này góp phần quan trọng trong quá trình viêm. Tế bào T hỗ trợ (Th) tham gia vào đáp ứng miễn dịch được chia thành hai nhóm chính là Th1 và Th2.
Trước đây, người ta cho rằng bệnh lý này chủ yếu liên quan đến đáp ứng miễn dịch qua trung gian Th2. Tuy nhiên, các nghiên cứu gần đây đã chỉ ra rằng đáp ứng miễn dịch trong bệnh lý này không hoàn toàn là do sự xuất hiện của tế bào Th2.
Cụ thể, sự tăng điều hòa của IL-13 và IFN-γ đã được ghi nhận, nhưng không có sự tham gia của IL-4, một cytokine đặc trưng cho Th2. Điều này cho thấy cơ chế miễn dịch của bệnh viêm loét đại trực tràng chảy máu phức tạp hơn và cần được nghiên cứu thêm để làm rõ.

4.3 Tế bào diệt tự nhiên
Tế bào diệt tự nhiên (Natural Killer T cell - NKT) là một dạng đặc biệt của tế bào T mang dấu ấn diệt tự nhiên, có khả năng sản xuất cả cytokine thuộc nhóm Th1 (ví dụ như IFN-γ) và nhóm Th2 (ví dụ như IL-5 hay IL-13).
Khi kháng nguyên glycolipid được trình diện cho tế bào diệt tự nhiên, các tế bào này sẽ kích hoạt quá trình phá hủy tế bào biểu mô, dẫn đến tổn thương và hình thành các vết loét. Đồng thời, IL-13 do tế bào này sản xuất không chỉ gây chết theo chương trình ở tế bào biểu mô mà còn tăng cường khả năng gây độc với các tế bào diệt tự nhiên.

5. Vai trò của Cytokine trong cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu
Cytokine là các tín hiệu truyền dẫn, đóng vai trò tăng cường và duy trì khả năng đáp ứng miễn dịch đặc hiệu trong bệnh viêm loét đại trực tràng chảy máu.
Bên cạnh các cytokine tiếp viên hay gặp như TNF-2, IL-1 hay IL-6, các cytokine khác do tế bào Th2 sản xuất như IL-10, IL-13 cũng có vai trò nhất định.
6. Vai trò của các cytokine tiền viêm
TNF-α đóng vai trò trung tâm trong việc khởi phát và duy trì quá trình viêm thông qua kích hoạt sản xuất IL-1β, IL-6, biệt hóa nguyên bào sợi và thúc đẩy hoạt hóa các tiền chất của yếu tố đông máu. Đồng thời, TNF-α cũng khởi động đáp ứng viêm cấp tính và quá trình chết tế bào theo chương trình.
Bên cạnh đó, TNF-α còn hoạt hóa đại thực bào, tế bào lympho, tế bào B và kích thích tế bào T tăng sản xuất IFN-γ. Ngoài ra, TNF-α khởi động con đường NF-κB, một con đường quan trọng trong biệt hóa, trưởng thành tế bào và kiểm soát sản xuất các cytokine tiền viêm.
Sự tăng sản xuất TNF-α sẽ dẫn đến tổn thương viêm ở hàng rào niêm mạc ruột, góp phần vào cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu.
IL-1 được sản xuất từ đại thực bào cũng đóng vai trò quan trọng trong cơ chế viêm với chức năng như một cytokine tiền viêm. IL-1 gồm hai dạng chính là IL-1α và IL-1β, giúp thúc đẩy sản xuất cyclooxygenase type 2, nitric oxide synthase, và phospholipase A.
Để kiểm soát viêm, chất đối kháng thụ thể IL-1 (IL-1Ra) sẽ điều hòa hoạt động của IL-1. Trong bệnh viêm loét đại trực tràng chảy máu, nếu nồng độ IL-1Ra tăng cao và tỉ lệ giữa IL-1Ra/IL-1 càng cao thì mức độ hoạt động của bệnh càng nặng. Ngoài ra, ở các bệnh nhân viêm ruột, mức tăng IL-1β ở niêm mạc đại tràng cũng được ghi nhận.
IL-6, một cytokine tiền viêm khác cũng được tìm thấy với nồng độ cao trong huyết thanh và mô của bệnh nhân mắc viêm loét đại trực tràng có chảy máu, đặc biệt trong các trường hợp bệnh nặng.
Điều này là do IL-6 liên kết với thụ thể sIL-6R để hình thành phức hợp, kích hoạt các tế bào bộc lộ protein gp130 trên bề mặt, từ đó hoạt hóa STAT3. Hoạt hóa STAT3 dẫn đến sự biểu hiện các yếu tố kháng quá trình chết theo phương trình như Bcl-2 và Bcl-xL, giúp tế bào T kháng lại quá trình này. Sự tồn tại của các tế bào T này sẽ góp phần thúc đẩy viêm mạn tính.
IL-9 được sản xuất từ tế bào Th9 cũng chịu ảnh hưởng bởi TGF-β và IL-4 trong quá trình trưởng thành. Cytokine này tác động đến hàng rào biểu mô niêm mạc ruột thông qua điều hòa Claudin-2, một chất trung gian chính trong hiện tượng thoát dịch ở ruột.
Các nghiên cứu chỉ ra rằng IL-9 được bộc lộ quá mức trong mô viêm của bệnh nhân mắc viêm loét đại trực tràng chảy máu, và nồng độ IL-9 trong huyết thanh tương quan với mức độ nặng của bệnh.
IL-13 là một cytokine đặc hiệu của Th2 được sản xuất bởi tế bào diệt tự nhiên, đóng vai trò quan trọng trong việc phá hủy lớp tế bào biểu mô ruột. IL-13 làm thay đổi tính thấm của niêm mạc ruột và ảnh hưởng đến vùng nối giữa các tế bào biểu mô, góp phần làm suy giảm chức năng hàng rào bảo vệ của ruột.
Ngoài ra, cytokine này còn làm giảm khả năng sửa chữa các tổn thương ở niêm mạc ruột, góp phần vào quá trình viêm mãn tính. IL-33 là một yếu tố tiền viêm mới và được coi như một chất “báo động” của hệ thống miễn dịch tại ruột.
IL-33 được sản xuất bởi các tế bào biểu mô niêm mạc ruột bị tổn thương và kích thích các phản ứng miễn dịch. Thụ thể của IL-33 có mặt trên bề mặt của các tế bào miễn dịch Th2, Th1 và cả tế bào điều hòa.
Nghiên cứu ban đầu về IL-33 ở bệnh nhân bị viêm loét đại trực tràng có chảy máu cho thấy rằng, nồng độ IL-33 trong cơ thể bệnh nhân cao hơn so với người khỏe mạnh bất kể bệnh đang ở giai đoạn ổn định hay hoạt động. Một nghiên cứu khác cũng cho thấy, sau khi điều trị bằng thuốc anti-TNF, sự bộc lộ IL-33 giảm đáng kể so với giai đoạn cấp tính.
7. Cytokine chống viêm và mối liên quan với cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu
TGF-β là một cytokine chống viêm, có vai trò quan trọng trong việc điều hòa và duy trì sự cân bằng giữa đáp ứng viêm và miễn dịch. Cytokine này hỗ trợ quá trình liền niêm mạc và bảo vệ niêm mạc ruột khỏi những thay đổi trong đường tiêu hóa, đặc biệt trong bệnh lý viêm loét đại trực tràng chảy máu.
IL-10 được sản xuất từ các tế bào B, tế bào T và tế bào đơn nhân, có chức năng ức chế sự sản xuất các cytokine gây viêm như TNF-α, IL-1β và IL-6. Vì lý do này, nồng độ IL-10 thường tăng cao ở bệnh nhân mắc viêm loét đại trực tràng có chảy máu, trong khi ở người khỏe mạnh, nồng độ IL-10 rất thấp và không thể phát hiện được. Hơn nữa, sự mất chức năng của thụ thể IL-10 do đột biến đã được chứng minh là có liên quan đến mức độ nặng của bệnh viêm loét đại trực tràng chảy máu.
8. Vai trò của một số cytokine khác
IL-8 là một cytokine điển hình khi có vai trò quan trọng trong việc hóa ứng động bạch cầu đa nhân đến thành ống tiêu hóa. IL-8 được sản xuất bởi nhiều loại tế bào, bao gồm tế bào T, tế bào nội mô, nguyên bào sợi, nhưng chủ yếu là các tế bào đơn nhân và đại thực bào.
Cytokine này xuất hiện nhiều ở các vùng niêm mạc bị tổn thương, từ đó thu hút các tế bào viêm, đặc biệt là bạch cầu đa nhân tập trung tại các khu vực này. Điều này phần nào giải thích cơ chế gây tổn thương viêm cấp và có thể dẫn đến hình thành các ổ vi áp xe ở niêm mạc ruột trong các bệnh lý viêm ruột.
Cơ chế bệnh sinh của bệnh viêm loét đại trực tràng chảy máu khá phức tạp và cho đến nay, chưa có phương pháp điều trị hoàn toàn khỏi căn bệnh này. Bệnh nhân thường được khuyến cáo duy trì một chế độ dinh dưỡng hợp lý cho hệ tiêu hóa, tránh căng thẳng và thường xuyên khám sức khỏe định kỳ để phát hiện bệnh kịp thời.
Hiện nay, chuyên khoa Nội tiêu hóa - Bệnh viện Đa khoa Quốc tế Vinmec không ngừng cập nhật các trang thiết bị hiện đại cùng đội ngũ bác sĩ chuyên gia, giúp thực hiện các xét nghiệm nội soi chính xác để chẩn đoán các bệnh lý về dạ dày, đại tràng như viêm, loét, polyp, ung thư, tìm vi khuẩn HP và phát hiện ung thư đường tiêu hóa sớm. Từ đó, bệnh viện có thể đưa ra hướng điều trị phù hợp cho từng bệnh nhân.
Tài liệu tham khảo
- NagreF, Gionchetti PR, Eliakim R. và cộng sự. (2017). Third European Evidence-based consensus on Diagnosis and Management of Ulcerative Colitis. Part 1: Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and lleo- anal Pouch Disorders. J Crohns Colitis, 11(6), 649-670.
- De Dombal F.T. (1968), Ulcerative colitis: definition, historical background, aetiology, diagnosis, naturel history and local complications, Postgrad Med J,44(515), 684-692.
- Crohn B.B. (1962). An historic note on ulcerative colitis. Gastroenterology, 42, 366-367.
- Lichtenstein G.R., btv. (2014), Medical Therapy of Ulcerative Colitis, Springer-Verlag, New York.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.