Bài viết bởi Thạc sĩ, Bác sĩ Mai Viễn Phương - Trưởng đơn nguyên Nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
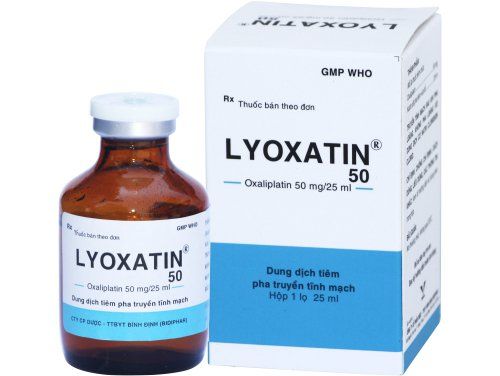
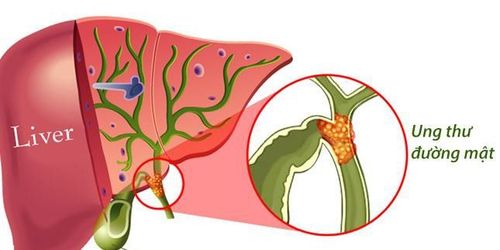
FDA đã cấp phép nhanh chóng cho dược phẩm infigratinib (Truseltiq, QED Therapeutics) để điều trị cho người lớn bị ung thư đường mật tiến triển tại chỗ hoặc di căn đã được điều trị trước đó với sự dung hợp yếu tố tăng trưởng nguyên bào sợi 2 ( FGFR2 ) hoặc sự sắp xếp lại khác.
FDA cũng đã phê duyệt cho FoundationOne CDx (Foundation Medicine) làm xét nghiệm chẩn đoán đồng hành để chọn bệnh nhân điều trị bằng infigratinib. Milind Javle, MD - một giáo sư về ung thư đường tiêu hóa tại Đại học The University of Trung tâm Ung thư Texas MD Anderson, ở Houston và điều tra viên chính của thử nghiệm dựa trên sự chấp thuận. Trong nghiên cứu, infigratinib cho thấy hứa hẹn là một lựa chọn điều trị mục tiêu cho bệnh nhân ung thư đường mật do dung hợp FGFR2, với đặc điểm an toàn được dung nạp tốt phù hợp với các quan sát trước đây ở nhóm bệnh nhân này. Tiến sĩ Javle, người đã trình bày dữ liệu thử nghiệm cho biết thêm tại Hội nghị chuyên đề về Bệnh ung thư đường tiêu hóa ảo năm 2021.
1. Nghiên cứu chỉ ra điều gì?
Trong nghiên cứu đa trung tâm, nhãn mở, một nhánh, giai đoạn 2 được gọi là CBGJ398X2204 (Số nhận dạng ClinicalTrials.gov: NCT02150967) —108 bệnh nhân đã trải qua ít nhất một lần điều trị ung thư đường mật tiến triển đã nhận được 125mg infigratinib mỗi ngày trong 21 ngày 28 chu kỳ-ngày cho đến khi nhiễm độc không thể chấp nhận được hoặc bệnh tiến triển. Trong số những bệnh nhân này, 107 (99%) bị ung thư đường mật giai đoạn IV. Tất cả các bệnh nhân đã được điều trị dự phòng bằng thuốc sevelamer chất kết dính phốt phát đường uống. Các thước đo kết quả hiệu quả chính là tỷ lệ đáp ứng tổng thể (ORR) và thời gian đáp ứng (DOR), được xác định bằng đánh giá trung tâm độc lập bị mù theo RECIST (Tiêu chí đánh giá đáp ứng trong khối u rắn) phiên bản 1.1.
Điểm kết thúc chính của nghiên cứu chứng minh ORR được xác nhận là 23% (KTC 95%, 16% -32%), với một câu trả lời hoàn toàn và 24 câu trả lời một phần. Nghiên cứu cũng cho thấy DOR trung bình là 5,0 tháng (KTC 95%, 3,7-9,3 tháng). Trong số 23 người trả lời, tám bệnh nhân duy trì phản ứng trong sáu tháng hoặc hơn.

2. Các tác dụng ngoại ý
Các tác dụng ngoại ý thường xảy ra nhất (tỷ lệ mắc bệnh ≥20%) là tăng phosphat huyết, tăng creatinine, nhiễm độc móng, viêm miệng, khô mắt, mệt mỏi, rụng tóc, hội chứng rối loạn cảm giác lòng bàn tay-thực vật, đau khớp, rối loạn tiêu hóa, táo bón, đau bụng, khô miệng, thay đổi lông mi, tiêu chảy, khô da, giảm cảm giác thèm ăn, mờ mắt và nôn mửa.
Những rủi ro nghiêm trọng liên quan đến infigratinib bao gồm tăng phosphat máu và bong tróc biểu mô sắc tố võng mạc. Theo dõi các tác dụng phụ này trong quá trình điều trị được khuyến cáo.
Xem thêm: Hướng dẫn chẩn đoán ung thư đường mật
Tài liệu tham khảo:
Dựa trên thông cáo báo chí từ FDA và QED Therapeutics (BridgeBio Pharma) và gastroendonews.com
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.