Bài viết của Thạc sĩ, Bác sĩ Mai Viễn Phương - Bác sĩ nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
Các kỹ thuật EMR trong cắt polyp ống tiêu hóa có thể được chia thành kỹ thuật hút và cắt (hút) hoặc nâng và cắt (không hút). Tuy nhiên, trong một số trường hợp nhất định, cả hai kỹ thuật đều được sử dụng cùng nhau.
1. Đặt vấn đề
Nhiều bệnh ung thư đường tiêu hóa được chẩn đoán ở giai đoạn cuối, cần phải phẫu thuật lớn có liên quan đến tỷ lệ mắc bệnh và tử vong đáng kể. Kết quả của những trường hợp này là không tối ưu do di căn tại chỗ hoặc di căn xa. Cắt niêm mạc nội soi được phát triển ở Nhật Bản để kiểm soát ung thư dạ dày giai đoạn đầu. Điều này đã được chấp nhận rộng rãi hơn một lựa chọn điều trị cho các tổn thương đường tiêu hóa khác nhau trên toàn cầu.
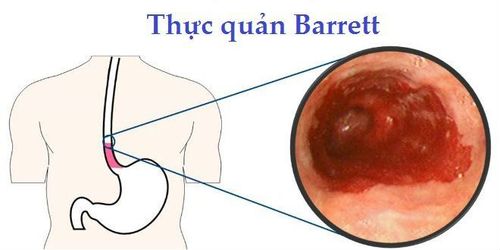
Các chỉ định đã mở rộng bao gồm điều trị loạn sản Barrett, loạn sản vảy thực quản, u tuyến ruột non và đại trực tràng. Cắt bỏ niêm mạc qua nội soi (EMR) cũng có ưu điểm là cung cấp dữ liệu cho việc đánh giá giai đoạn chính xác tại chỗ của bệnh so với các liệu pháp bóc tách, như đốt bằng argon plasma (APC), liệu pháp quang động hoặc cắt bỏ bằng sóng cao tần (RFA). Tuy nhiên, kỹ thuật cắt polyp ống tiêu hóa cần có chuyên môn và đào tạo đầy đủ để an toàn và hiệu quả.
2. Phân loại hình thái của khối u bề ngoài
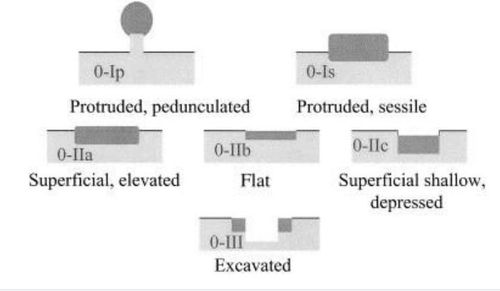
Tổn thương tân sinh trong đường tiêu hóa được gọi là ở bề mặt khi hình ảnh nội soi của chúng gợi ý rằng, sự xâm lấn giới hạn ở niêm mạc và lớp dưới niêm mạc. Hiệp hội Ung thư dạ dày Nhật Bản đã phát triển một hướng dẫn phân loại ung thư dạ dày tiến triển từ loại 1-5. Sau đó, loại 0 được thêm vào để mô tả các tổn thương bề ngoài.
Loại 0-I lại được chia nhỏ thành các tổn thương có cuống (0-Ip) và không cuống (0-Is). Loại 0-II được chia thành ba loại phụ; 0-IIa biểu thị tổn thương hơi cao, 0-IIb biểu thị tổn thương phẳng và 0-IIc đặc trưng cho tổn thương lõm xuống. Loại 0-III là một tổn thương lõm xuống. Các kết hợp khác nhau của phân loại này có thể được sử dụng để mô tả các tổn thương hỗn hợp cao, phẳng hoặc lõm.
Ví dụ, một tổn thương phẳng và lõm xuống, không lồi lõm, không có sẹo được mô tả là loại 0-IIb/c. Mặc dù những biểu hiện này chủ yếu được mô tả trong ung thư dạ dày, phân loại tương tự được điều chỉnh cho phù hợp với các tổn thương bề mặt của thực quản và ruột già. Trong tổn thương loại 0-I, đường kính là tiêu chí dự đoán đáng tin cậy vì nguy cơ xâm lấn dưới niêm mạc tăng theo đường kính. Tuy nhiên, với các tổn thương loại 0-II, các dạng phụ hình thái có tầm quan trọng lớn hơn. Sự xâm lấn của lớp dưới niêm mạc thường xuyên hơn ở các tổn thương lõm (0-IIc). Tỷ lệ xâm lấn dưới niêm mạc cao ở các tổn thương loại 0-III. Nội soi nhuộm màu và các công nghệ hình ảnh điện tử hoặc quang học nâng cao như hình ảnh dải hẹp (NBI) sẽ hữu ích để xác định đặc điểm của các tổn thương này.
3. Giai đoạn của các tổn thương
Đánh giá giai đoạn chính xác tại chỗ sẽ ra lý tưởng trước khi thực hiện EMR trong cắt polyp ống tiêu hóa. Tuy nhiên, điều này không dễ đạt được trong nhiều trường hợp. Chụp cắt lớp vi tính (CT) được thực hiện để loại trừ di căn xa và các nghiên cứu khác nhau đã chỉ ra rằng, di căn xa hầu như không tồn tại trong ung thư còn khu trú ở lớp niêm mạc. Một nghiên cứu tiền cứu trên 100 bệnh nhân bị ung thư sớm Barrett cho thấy, CT không ảnh hưởng đến phân loại TNM. Tuy nhiên, nguy cơ di căn tăng lên khi xâm lấn dưới niêm mạc và trong những trường hợp này.
Siêu âm nội soi (EUS) là một công cụ rất chính xác để phân giai đoạn T và N của ung thư thực quản tiến triển. Tuy nhiên, giá trị của nó trong bệnh tân sinh sớm còn nhiều nghi vấn. Độ phân giải tiêu chuẩn EUS không đủ để phân biệt khối u bề mặt niêm mạc với khối u xâm lấn sâu. Tuy nhiên, EUS hữu ích trong phân đoạn N và độ chính xác được cải thiện đáng kể (90%) bằng cách bổ sung chọc hút kim nhỏ (FNA). Một nghiên cứu hồi cứu về vai trò của nội soi độ phân giải cao (HRE) và EUS trên 50 bệnh nhân mắc chứng tân sinh sớm Barrett cho thấy, tổn thương theo phân loại Paris 0-IIa hoặc 0-IIb có liên quan đến bệnh niêm mạc (83–100%) so với theo phân loại Paris 0 tổn thương -IIc (66%), nơi có nhiều khả năng xâm lấn vào lớp dưới niêm mạc.
Một nghiên cứu tiền cứu khác đã so sánh HRE với EUS độ phân giải cao trong ung thư thực quản giai đoạn đầu. Kết quả của nghiên cứu này đã chứng minh rằng, độ chính xác chẩn đoán tổng thể của HRE và EUS độ phân giải cao là cao (khoảng 80%), không có sự khác biệt đáng kể giữa hai kỹ thuật. Tuy nhiên, độ chính xác chẩn đoán không đạt yêu cầu, đặc biệt trong việc phân biệt bệnh niêm mạc với bệnh dưới niêm mạc. Một đầu dò nhỏ EUS với tần số lên đến 20–30 MHz là cần thiết để phân biệt các lớp niêm mạc và lớp dưới niêm mạc, tuy nhiên kết quả cũng không hoàn toàn khả quan. Đối với ung thư biểu mô dạ dày, độ chính xác của việc phát hiện xâm nhập sm1 là 65–79%.
4. Đánh giá mô học
Một trong những yếu tố tiên lượng quan trọng nhất của di căn hạch là độ thâm nhiễm của tổn thương. Tổn thương niêm mạc được chia nhỏ thành T1m1, nơi bệnh giới hạn ở lớp biểu mô bề ngoài, T1m2 nơi bệnh liên quan đến lớp đệm và T1m3 kéo dài cũng như liên quan đến cơ niêm mạc. Tương tự, sự tham gia của lớp dưới niêm mạc được chia nhỏ thành T1sm1, T1sm2 và T1sm3, bằng chứng là sự tham gia của một phần ba bề mặt, một phần ba giữa và một phần ba sâu nhất của lớp dưới niêm mạc. Tỷ lệ di căn hạch bạch huyết liên quan đến niêm mạc là không đáng kể (T1m1 – m3) và do đó những tổn thương này có thể thích hợp để xử trí điều trị nội soi, trong khi những tổn thương có liên quan dưới niêm mạc làm tăng khả năng di căn hạch bạch huyết, dao động từ 0-8% ở T1sm1 đến 26 –67% ở các tổn thương T1sm2–3. Do đó, xâm lấn sâu dưới niêm mạc được coi là chỉ định cho phẫu thuật và EMR trong cắt polyp ống tiêu hóa để xác định vị trí cục bộ chính xác.
5. Kỹ thuật cắt nội soi
Các kỹ thuật EMR cắt polyp ống tiêu hóa có thể được chia thành kỹ thuật hút và cắt (hút) hoặc nâng và cắt (không hút). Tuy nhiên, trong một số trường hợp nhất định, cả hai kỹ thuật đều được sử dụng cùng nhau. Trong kỹ thuật nâng và cắt, một mũi tiêm dưới niêm mạc được sử dụng để tách lớp đệm cơ ra khỏi tổn thương và điều này sẽ làm giảm nguy cơ thủng. Trong trường hợp tổn thương xâm lấn, một dấu hiệu không nâng được tổn thương lên xuất hiện rõ ràng sau khi tiêm vào lớp dưới niêm là khả năng xâm lấn sâu hơn vào tổn thương, do đó không thể thực hiện EMR. EMR đại tràng thường được thực hiện bằng phương pháp không hút và dùng một cái thòng lọng để cắt polyp sau khi tiêm dưới niêm mạc.
6. Các dung dịch được sử dụng
Nhiều dung dịch khác nhau được sử dụng để tiêm dưới niêm mạc. Nước muối thông thường là tác nhân được sử dụng rộng rãi nhất, nhưng nó được hấp thụ nhanh chóng. Để khắc phục điều này, người ta thường sử dụng các tác nhân khác như nước muối ưu trương, 50% dextrose, sodium hyaluronate, 4% succinylated gelatine,... Tiêm được thực hiện bằng kim tiêm tại một hoặc nhiều vị trí xung quanh tổn thương.
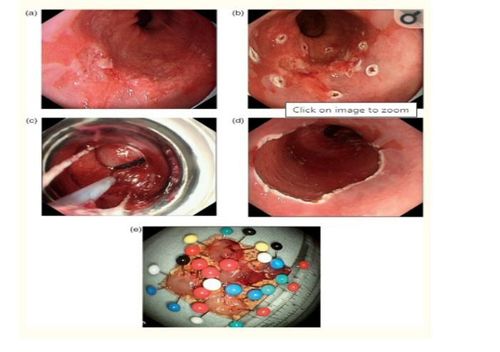
7. Chỉ định cắt niêm mạc nội soi điều trị trong ung thư đường tiêu hóa giai đoạn đầu.
Bảng chỉ định cắt niêm mạc nội soi điều trị trong ung thư đường tiêu hóa giai đoạn đầu:

8. EMR đặc biệt hữu ích trong việc quản lý các tổn thương lớn không cuống và phẳng của đại trực tràng.
Polyp có kích thước lớn hơn 2 cm có thể được cắt từng đoạn để tránh thủng. Tuy nhiên, có những lo ngại liên quan đến việc đánh giá mô học không đầy đủ và tỷ lệ tái phát cao hơn sau khi cắt bỏ từng phần. Trong 148 trường hợp polyp lớn và khổng lồ, EMR được thực hiện theo từng khối trong 44% trường hợp và từng phần trong số còn lại. Tỷ lệ tái phát là 4,2% sau thời gian theo dõi trung bình là 30 tháng.
Một nghiên cứu thứ hai bao gồm 186 polyp được cắt bỏ nội soi có đường kính tối đa từ 3 đến 13 cm. Trong số 141 polyp không cuống được cắt bỏ, có hai bệnh nhân phải phẫu thuật vì chảy máu trong thủ thuật và một bệnh nhân do thủng manh tràng muộn. Trong thời gian theo dõi trung bình 40 tháng, chỉ 3% bệnh nhân tái phát bệnh lành tính. Tuy nhiên, một phân tích tổng hợp gần đây bao gồm 25 nghiên cứu cho thấy tỷ lệ tổng hợp thấp hơn của các trường hợp cắt bỏ hoàn toàn điều trị khỏi bệnh ở mức 59%. Theo các nghiên cứu cho thấy, tỷ lệ tái phát polyp sau khi cắt bỏ toàn bộ ít hơn 60% so với cắt từng phần và việc sử dụng thêm APC không cải thiện tỷ lệ tái phát. Tuy nhiên, một thử nghiệm ngẫu nhiên trước đó cho thấy rằng sự tái phát polyp sau khi cắt bỏ hoàn toàn các khối polyp lớn sẽ giảm đáng kể khi sử dụng APC.
9. Các biến chứng cắt polyp ống tiêu hóa
Chảy máu và thủng là những biến chứng chính liên quan đến EMR trong cắt polyp ống tiêu hóa. Trong các trường hợp EMR qua thực quản, không có sự khác biệt về các biến chứng khi kỹ thuật chụp EMR được so sánh với thắt và cắt. Trong 100 trường hợp EMR, chỉ có hai bệnh nhân bị chảy máu nhẹ và không có lỗ thủng.
Một khiếm khuyết niêm mạc liên quan đến hơn 3/4 chu vi của thực quản sau EMR có liên quan đáng kể đến sự phát triển tiếp theo của hẹp thực quản. Chảy máu là biến chứng phổ biến nhất xảy ra ở 7–8% bệnh nhân đang điều trị EMR hoặc ESD tiêu chuẩn cho EGC. Các lỗ thủng không phổ biến trong EMR dạ dày so với ESD (4%). Liều cao của thuốc ức chế bơm proton thường được dùng trong 4-8 tuần để tạo điều kiện làm lành niêm mạc sau EMR đường tiêu hóa trên. Bệnh nhân thường chỉ được truyền dịch trong 24 giờ, sau đó là chế độ ăn mềm trong 3 ngày.
Tiêm đủ lượng chất lỏng dưới niêm mạc là điều tối quan trọng để tránh thủng đại tràng, đặc biệt là ở những tổn thương bên phải. Một loạt kỹ thuật EMR đại tràng gần đây ở 182 trường hợp tổn thương cho thấy tỷ lệ thủng là 1% và chảy máu trong 12% trường hợp. Các biến chứng nhỏ và thường xuyên hơn bao gồm đau và hội chứng sau cắt polyp.
10. Phần kết luận
EMR là tiến bộ quan trọng trong lĩnh vực nội soi điều trị và đã được chấp nhận như một phương pháp thay thế xâm lấn tối thiểu cho phẫu thuật trong các tổn thương niêm mạc ảnh hưởng đến đường tiêu hóa trên và dưới. Kinh nghiệm lớn nhất chủ yếu là từ các bác sĩ nội soi Nhật Bản, nhưng các chỉ định đã được mở rộng để phù hợp với các bệnh chủ yếu của phương Tây như Barrett thực quản. EUS có thể hữu ích để đánh giá giai đoạn nốt của ung thư sớm. Tuy nhiên, vai trò của nó trong việc phân biệt ung thư niêm mạc và ung thư dưới niêm mạc còn nhiều nghi vấn. Hình thái học qua nội soi là một hướng dẫn hữu ích để đánh giá các tổn thương có thể phù hợp với EMR. Các thủ thuật này có nguy cơ biến chứng cao nên cần được thực hiện bởi các bác sĩ nội soi có kinh nghiệm và được đào tạo.
Tài liệu tham khảo:
Jayan Mannath, MD, MRCP, Endoscopic mucosal resection: who and how? Therap Adv Gastroenterol. 2011 Sep; 4(5): 275–282.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.