Bài viết bởi Tiến sĩ, Bác sĩ Trương Ngọc Hải - Bác sĩ Hồi sức - Khoa Hồi sức cấp cứu - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Ngày nay, với gần 180 dấu ấn sinh học đã được xác định, nhiều dấu ấn sinh học đang được các bác sĩ sử dụng để phát hiện, theo dõi diễn biến, đánh giá tiên lượng của tình trạng nhiễm khuẩn, nhiễm khuẩn huyết và quyết định ngừng thuốc kháng sinh. Tuy nhiên, các dấu ấn sinh học này có thể bị thải trừ trong quá trình lọc máu liên tục, ảnh hưởng đến độ tin cậy trong xác định mức độ nghiêm trọng của tình trạng nhiễm khuẩn. Cho đến nay, các chuyên gia vẫn đang nỗ lực tìm kiếm dấu ấn sinh học mới không bị thải trừ qua CRRT.
1. Các dấu ấn sinh học được sử dụng thường xuyên nhất trên lâm sàng
1.1. C-reactive Protein
C-reactive Protein (CRP) chủ yếu hiện diện dưới dạng monome (mCRP) trong máu của bệnh nhân nhiễm khuẩn huyết [5], do trọng lượng phân tử tương đối nhỏ (22- 25 kDa) nên được thải trừ trong tất cả các phương thức CRRT [4]. Ngoài ra, một lượng đáng kể mCRP cũng được hấp phụ trên màng lọc [2, 6]. Hiện nay, nhiều khoa Hồi sức cấp cứu sử dụng các màng lọc có tính hấp phụ cao càng tăng thải trừ mCRP. Nồng độ trong huyết tương của C-reactive Protein có thể thấp giả tạo trong quá trình CRRT, nên nồng độ CRP không đáng tin cậy trong chẩn đoán hoặc đánh giá mức độ nhiễm khuẩn trong quá trình CRRT [7].
1.2. Procalcitonin (PCT)
Ở những bệnh nhân nhiễm khuẩn huyết được lọc máu tĩnh-tĩnh mạch liên tục (CVVH), PCT được phát hiện trong dịch siêu lọc của tất cả các bệnh nhân [10]. Hầu hết lượng PCT sẽ được thải trừ qua dòng dịch đối lưu, nhưng cơ chế hấp phụ cũng góp phần thải trừ PCT trong những giờ đầu điều trị [10]. Sử dụng các màng lọc có tính hấp phụ cao càng gia tăng hơn nữa thải trừ CRP và PCT [6, 11].
1.3. Brain Natriuretic Factors
Dấu ấn sinh học BNP và NT-proBNP được ứng dụng gần đây trong nhiễm khuẩn huyết. Cả hai dấu ấn sinh học BNP và NT-proBNP đều bị thải trừ rất dễ dàng qua các loại màng lọc high-flux và low-flux trong CRRT do kích thước phân tử thấp của chúng [13], [14].
2. Các dấu ấn sinh học Cytokine/Chemokine trong nhiễm khuẩn huyết
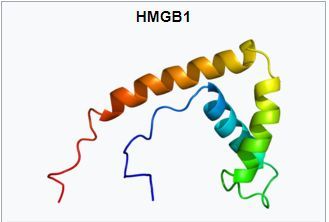
2.1. High Mobility Group 1 Protein (HMGB-1)
Mặc dù HMGB-1 có trọng lượng phân tử tương đối thấp nên về lý thuyết HMGB-1 có thể bị thải trừ qua cơ chế lọc đối lưu. Tuy nhiên, thực tế HMGB-1 chỉ được thải trừ hiệu quả thông qua cơ chế hấp phụ bằng các loại màng lọc có tính hấp phụ cao, đặc biệt là màng lọc được xử lý bề mặt acrylonitrile 69 (AN69-ST) [15].
2.2. Osteopontin
Osteopontin là một protein tích điện âm, có trọng lượng phân tử khoảng 32 kDa. Chưa có bằng chứng thuyết phục lọc máu liên tục có thể thải trừ Osteopontin trong hệ tuần hoàn [16]. Tuy nhiên, CRRT sử dụng các loại màng lọc mới, ví dụ màng lọc AN69-ST – do có bề mặt phủ lớp biopolymer polyethylen nên có mật độ điện tích dương cao, ngoài khả năng tương thích sinh học và tính thấm cao, màng này còn có khả năng hấp phụ mạnh nên có thể gia tăng thải trừ Osteopontin [6].
3. Dấu ấn sinh học trong nhiễm khuẩn huyết có liên quan đến tổn thương nội mô mạch máu – Endocan
Endocan là một loại dermatan sulfate proteoglycan hòa tan có nguồn gốc nội mô mới, có khối lượng phân tử khoảng 15-40 kDa [17, 18]. Các màng lọc CRRT hiện đại có thể thải trừ các chất có trọng lượng phân tử tới 35 kDa. Khi sử dụng màng lọc mới có tính hấp phụ cao, càng gia tăng khả năng thải trừ endocan qua CRRT [6]. Do đó, mức độ tin cậy của endocan trong CRRT có thể bị thay đổi.
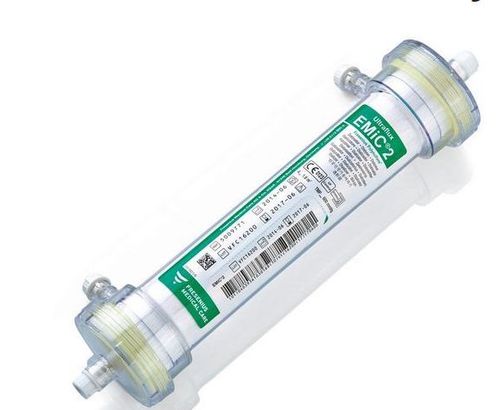
4. Dấu ấn sinh học trong nhiễm khuẩn huyết có liên quan đến dãn mạch – Proadrenomedullin (MR-proADM)
Trọng lượng phân tử của MR-proADM là từ 4 đến 5,5 kDa, nên cũng có thể bị CRRT loại bỏ. Nghiên cứu của Mueller và cộng sự cho thấy sự sụt giảm đáng kể của MR-proADM (45, 65%) nếu sử dụng màng lọc high-flux [20] (đặc biệt là với ngưỡng lọc 35 kDa của các màng lọc CRRT hiện đại [6]). Cần có thêm các nghiên cứu xác định có hay không khả năng thải trừ MR-proADM bằng cơ chế đối lưu trong CRRT.
5. Dấu ấn sinh học khác trong giai đoạn cấp tính – Pentraxin
Pentraxin-3 (PTX3) là một glycoprotein được các tế bào nội mô và tế bào viêm phóng thích khi nhận kích hoạt của cytokine và endotoxin. PTX3 phản ánh tình trạng viêm của các mạch máu tại chỗ và tải lượng vi khuẩn tốt hơn CRP [23]. Do đó, PTX3 có thể là một dấu hiệu thích hợp hơn CRP về phản ánh mức độ nghiêm trọng và tiên lượng của nhiễm khuẩn mô mềm hoại tử. Theo báo cáo của Hansen, mối liên quan có ý nghĩa thống kê giữa nồng độ PTX3 cao và sự xuất hiện của sốc nhiễm khuẩn, cắt cụt chi, nhu cầu lọc máu và nguy cơ tử vong ở bệnh nhân bị nhiễm khuẩn hoại tử mô mềm [23].
Hầu hết ở các bệnh nhân, PTX3 trong huyết tương ở dạng đơn phân có trọng lượng phân tử khoảng 35 kDa [23] và do đó trên lý thuyết có thể được thải trừ bằng CRRT. Gần đây, Schilder và cộng sự đã chứng minh tuy PTX3 được hấp phụ một ít nhưng phương thức CVVH không thải trừ được PTX3 bằng cơ chế đối lưu, dẫn đến nồng độ PTX3 trong huyết tương không thay đổi [24]. Cần nghiên cứu thêm khả năng tăng thải trừ PTX3 với phương thức CVVH sử dụng các loại màng lọc có đặc tính hấp phụ cao [24, 25].
6. Dấu ấn sinh học nhóm dấu ấn tế bào trong nhiễm khuẩn huyết – Presepsin
Gần đây, sCD14-ST còn được gọi là presepsin, đã được xác định là một dấu ấn sinh học tiềm năng của nhiễm khuẩn huyết [26]. Presepsin được phân mảnh từ một glycoprotein lớn hơn và có trọng lượng phân tử khoảng 13 kDa. Độ thanh thải của presepsin có thể còn cao hơn dự kiến vì phân tử này có thể “kết dính” vào màng lọc có tính hấp phụ cao [6].
7. Dấu ấn sinh học về đông máu trong nhiễm khuẩn huyết - Heparin Binding Protein
Heparin Binding Protein (HBP) còn được gọi là protein kháng khuẩn mang điện tích dương, có trọng lượng phân tử là 37 kDa [28] và do đó có thể được CRRT thải trừ thông qua cơ chế đối lưu [6]. Sử dụng các màng lọc có tính hấp phụ cao có thể giúp tăng cường khả năng thải trừ HBP thông qua cơ chế hấp phụ [6].
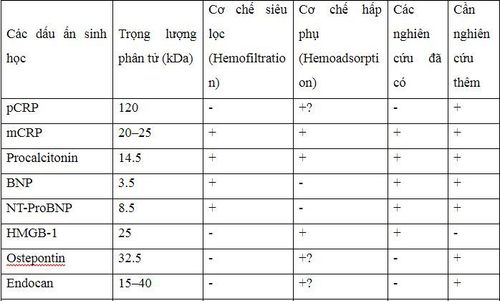
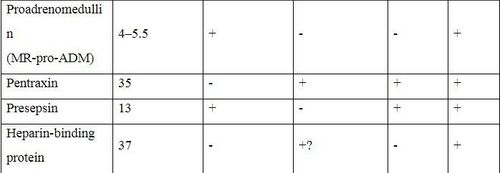
Bảng sau đây tóm tắt tất cả các dấu ấn sinh học được mô tả trong tổng quan này với thông tin về trọng lượng phân tử, khả năng thải trừ bằng cơ chế đối lưu và/hoặc hấp phụ, ghi nhận nghiên cứu đã có và cần nghiên cứu thêm. Qua đó cho thấy, các dấu ấn sinh học đều có thể được thải trừ qua CRRT, đặc biệt khi sử dụng màng lọc có tính hấp phụ cao. Vì vậy chưa có bất kỳ dấu ấn sinh học nào phản ánh chính xác tình trạng nhiễm khuẩn ở bệnh nhân đang được CRRT. Cần thực hiện nhiều nghiên cứu để đánh giá, tìm ra dấu ấn sinh học mới đáng tin cậy phản ánh tình trạng nhiễm khuẩn trong quá trình CRRT. Nhiệm vụ này còn trở nên phức tạp hơn khi màng lọc có tính hấp phụ cao đã nâng ngưỡng lọc lên tới 65 kDa.
Tài liệu tham khảo
1.Pierrakos C, Vincent JL. Sepsis biomarkers: a review. Crit Care. 2010;14:R15.
2. Honore PM, Jacobs R, De Waele E, Van Gorp V, Spapen HD. Biomarkers of inflammation during continuous renal replacement therapy: sensors, players, or targets? Blood Purif.
2014;38:102–3.
3. Tillett WS, Francis T. Serological reactions in pneumonia with a non-protein somatic fraction
of pneumococcus. J Exp Med. 1930;52:561–71.
4. McFadyen JD, Kiefer J, Braig D, et al. Dissociation of C-reactive protein localizes and amplifes inflammation: evidence for a direct biological role of C-reactive protein and its conformational changes. Front Immunol. 2018;9:1351.
5. Taylor KE, van den Berg CW. Structural and functional comparison of native pentameric,
denatured monomeric and biotinylated C-reactive protein. Immunology. 2007;120:404–11.
6. Dahaba AA, Elawady GA, Rehak PH, List WF. Procalcitonin and proinflammatory cytokine
clearance during continuous venovenous haemofltration in septic patients. Anaesth Intensive
Care. 2002;30:269–74.
7. Matsui T, Nakagawa T, Kikuchi H, Horio H, Hashimura K. The effect of continuous renal
replacement therapy with the AN69ST membrane on inflammatory markers and the level of
consciousness of hemodialysis patients with stroke: comparison with hemodialysis with low
blood flow rate. Pril (Makedon Akad Nauk Umet Odd Med Nauki). 2018;39:29–35.
8. Taylor R, Jones A, Kelly S, et al. A review of the value of procalcitonin as a marker of infection. Cureus. 2017;9:e1148.
9. Vijayan AL, Ravindran S, Saikant R, Lakshmi S, Kartik R. Procalcitonin: a promising diagnostic marker for sepsis and antibiotic therapy. J Intensive Care. 2017;5:51.
10. Level C, Chauveau P, Guisset O, et al. Mass transfer, clearance and plasma concentration of
procalcitonin during continuous veno-venous hemofltration in patients with septic shock and
acute oliguric renal failure. Crit Care. 2003;6:R160–6.
11. Honore PM, Jacobs R, Joannes-Boyau O, et al. Newly designed CRRT membranes for sepsis and SIRS—a pragmatic approach for bedside intensivists summarizing the more recent
advances: a systematic structured review. ASAIO J. 2013;59:99–106.
12. N L, Zhang Y, Fan S, Xing J, Liu H. BNP and NT-proBNP levels in patients with sepsis. Front Biosci (Landmark Ed). 2013;18:1237–43.
13. Pirracchio R, Salem R, Mebazaa A. Use of B natriuretic peptide in critically ill patients.
Biomark Med. 2009;3:541–7.
14. Wahl HG, Graf S, Renz H, Fassbinder W. Elimination of the cardiac natriuretic peptides
B-type natriuretic peptide (BNP) and N-terminal proBNP by hemodialysis. Clin Chem.
2004;50:1071–4.
15. Yumoto M, Nishida O, Moriyama K, et al. In vitro evaluation of high mobility group box
1 protein removal witvarious membranes for continuous hemofltration. Ther Apher Dial. 2011;15:385–93.
16. Honore PM, Jacobs R, Hendrickx I, De Waele E, Van Gorp V, Spapen HD. To counteract or to clear high-mobility group box-1 protein in influenza A (H1N1) infection? That may become
the question. Crit Care. 2015;19:401.
17. Honore PM, De Bels D, Attou R, Redant S, Gallerani A, Kashani K. Endocan removal during continuous renal replacement therapy: does it affect the reliability of this biomarker? Crit Care.2019;23:184.
18. Hureau M, Gaudet A, De Freitas Caires N, et al. Endocan is a reliable biomarker during continuous renal replacement therapy. Crit Care. 2019;23:296.
19. De Freitas Caires N, Gaudet A, Portier L, Tsicopoulos A, Mathieu D, Lassalle P. Endocan,
sepsis, pneumonia, and acute respiratory distress syndrome. Crit Care. 2018;22:280.
20. Mueller T, Gegenhuber A, Kronabethleitner G, Leitner I, Haltmayer M, Dieplinger B. Plasma concentrations of novel cardiac biomarkers before and after hemodialysis session. Clin
Biochem. 2015;48:1163–6.
21. Elke G, Bloos F, Wilson DC, et al. The use of mid-regional proadrenomedullin to identify
disease severity and treatment response to sepsis—a secondary analysis of a large randomised
controlled trial. Crit Care. 2018;22:79.
22. Honore PM, De Bels D, Attou R, Redant S, Kashani K. The challenge of removal of sepsis
markers by continuous hemofltration. Crit Care. 2019;23:173.
23. Hansen MB, Rasmussen LS, Garred P, Bidstrup D, Madsen MB, Hyldegaard O. Pentraxin-3 as a marker of disease severity and risk of death in patients with necrotizing soft tissue infections: a nationwide, prospective, observational study. Crit Care. 2016;20:40.
24. Schilder L, Nurmohamed SA, ter Wee PM, et al. Putative novel mediators of acute kidney
injury in critically ill patients: handling by continuous venovenous hemofltration and effect of
anticoagulation modalities. BMC Nephrol. 2015;16:178.
25. Honore PM, Spapen HD. Pentraxin-3 to better delineate necrotizing soft tissue infection: not
really! Crit Care. 2016;20:173.
26. Zhang X, Liu D, Liu YN, Wang R, Xie LX. The accuracy of presepsin (sCD14-ST) for the
diagnosis of sepsis in adults: a meta-analysis. Crit Care. 2015;19:323.
27. Honore PM, Jacobs R, Hendrickx I, De Waele E, Van Gorp V, Spapen HD. Presepsin and
sepsis-induced acute kidney injury treated with continuous renal replacement therapy: will
another promising biomarker bite the dust? Crit Care. 2015;19:428.
28. Honore PM, De Bels D, Barreto Gutierrez L, Redant S, Spapen HD. Heparin-binding protein
in sepsis: player! predictor! positioning? Ann Intensive Care. 2019;9:71.
29. Tverring J, Vaara ST, Fisher J, Poukkanen M, Pettilä V, Linder A, FINNAKI Study Group.
Heparin-binding protein (HBP) improves prediction of sepsis-related acute kidney injury. Ann
Intensive Care. 2017;7:105.
30. Honore PM, Jacobs R, Hendrickx I, De Waele E, Van Gorp V, Spapen HD. ‘Biomarking’ infection during continuous renal replacement therapy: still relevant? Crit Care. 2015;19:232.
31. Schadler D, Pausch C, Heise D, et al. The effect of a novel extracorporeal cytokine hemoadsorption device on IL-6 elimination in septic patients: a randomized controlled trial. PLoS One. 2017;12:e0187015.
32. Honore PM, Hoste E, Molnár Z, et al. Cytokine removal in human septic shock: where are we and where are we going? Ann Intensive Care. 2019;9:56
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.