Bài viết bởi Tiến sĩ, Bác sĩ Trương Ngọc Hải - Khoa Hồi sức cấp cứu - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Trong hầu hết trường hợp, biến cố “Suy chức năng thận nhân tạo” có liên quan với tiến triển đông máu và/hoặc tắc nghẽn các thành phần của hệ thống lọc máu. Những tiến trình này có thể xảy ra đồng thời.
1. Cơ chế suy yếu thận nhân tạo trong điều trị thay thế thận nhân tạo
“Suy chức năng thận nhân tạo” là thuật ngữ được giới thiệu gần đây để mô tả biến cố kết thúc điều trị thay thế thận nhân tạo (ĐTTTTLT) [6]. Suy chức năng thận nhân tạo sớm là khi quá trình ĐTTTTLT phải dừng lại trước 72 giờ, biến cố này rất thường gặp trong thực hành lâm sàng. Trong hầu hết trường hợp, biến cố “Suy chức năng thận nhân tạo” có liên quan với tiến triển đông máu và/hoặc tắc nghẽn các thành phần của hệ thống lọc máu. Những tiến trình này có thể xảy ra đồng thời [2],[5].
1.1 Tắc nghẽn màng lọc
Tắc nghẽn màng lọc mô tả tiến trình bão hòa các lỗ trên màng lọc. Tắc nghẽn xảy ra thứ phát do lắng đọng chậm và liên tục protein và mảnh vụn hồng cầu trong lúc ĐTTTTLT. Tắc nghẽn dẫn đến giảm tính thấm của màng lọc và giảm hệ số sàng của các phân tử lớn hơn. Khi đó, áp lực xuyên màng gia tăng chậm và từ từ [36].
Tắc nghẽn lỗ lọc trên màng lọc có thể thúc đẩy hình thành cục máu đông thứ phát trong các sợi rỗng của quả lọc (Hình 1) [1], [5]. Tiến trình này dường như bị ảnh hưởng bởi tương tác giữa protein huyết tương, dòng chảy của máu, lưu lượng mao mạch và xuyên màng, đặc điểm màng và dịch truyền [5].
![Hình 1. Vị trí đông quả lọc [1]](/static/uploads/small_20201224_015822_658253_loc_max_1800x1800_jpg_e3b00f766a.jpg)
1.2 Hình thành máu đông trong hệ thống lọc máu
Máu tuần hoàn trong hệ thống ngoài cơ thể gây hoạt hóa dòng thác đông máu. Máu đông là nguyên nhân chính của suy chức năng thận nhân tạo [6]. Máu đông thường được thấy được nhiều nhất ở bầu bẫy khí và trong quả lọc, có thể hình thành một cách nhanh chóng hoặc từ từ và tiến triển (Hình 1). Ngoài ra, máu đông hình thành tại bầu bẫy khí gây cản trở máu trả về bệnh nhân. Hiện tượng này thường bị chẩn đoán nhầm là “quả lọc bị đông” (Hình 2) [1].
Máu đông tại bầu bẫy khí gây tăng áp lực máu về (dòng máu ra khỏi quả lọc) và áp lực trước quả lọc. Máu đông tại quả lọc gây tăng áp lực trước quả lọc. Tất cả đều làm tăng áp lực xuyên màng thứ phát [5].
![Hình 2: Vị trí đông bầu bẫy khí [1]](/static/uploads/20201224_015948_838653_2_max_1800x1800_jpg_786308e1b4.jpg)
2. Chiến lược tối ưu đời sống quả lọc mà không sử dụng thuốc kháng đông
2.1. Đường rút máu – trả máu
Đường rút máu – trả máu hoạt động tốt là một trong các yếu tố cần thiết trong thành công của ĐTTTTLT. Catheter sử dụng trong ĐTTTTLT là loại catheter tạm thời hoặc catheter lọc máu đường hầm có nút chặn. Bệnh nhân có bệnh thận mạn giai đoạn cuối không sử dụng rò động – tĩnh mạch (AVF) để rút – trả máu trong ĐTTTTLT. Vì thời gian lọc máu kéo dài và lưu lượng rút máu thấp làm tăng nguy cơ tuột kim và chảy máu [4].
Vị trí đặt catheter tối ưu được xác định bởi nguy cơ biến chứng khi thực hiện thủ thuật đặt catheter, khả năng tạo huyết khối, nguy cơ chít hẹp và nhiễm trùng. Tĩnh mạch cảnh trong phải thường là vị trí được lựa chọn đặt catheter tạm thời. Catheter cảnh trong bên phải ít ảnh hưởng đến lưu lượng máu hơn so với bên trái khi bệnh nhân di chuyển đầu vì catheter được tiếp cận trực tiếp vào tĩnh mạch chủ trên. Tĩnh mạch đùi là vị trí thường được lựa chọn thứ hai trong ĐTTTTLT. Tĩnh mạch dưới đòn không được khuyến cáo lựa chọn vì nguy cơ chít hẹp mạch máu và ảnh hưởng chức năng rò động – tĩnh mạch sau này [4].
Catheter không hoạt động tốt có nhiều nguyên nhân như huyết khối, gập catheter và tạo lớp màng fibrin quanh đầu tận catheter. Bơm tráng và khóa giữ heparin trong lòng catheter giúp ngăn ngừa tạo huyết khối bên trong. Lớp màng fibrin bên ngoài catheter cần sử dụng dụng cụ chải hoặc tước bỏ cơ học [4].
2.2. Màng lọc
Màng lọc sử dụng trong hệ thống lọc máu đặc trưng bởi thành phần, tính tương hợp sinh học, kích thước lỗ lọc, diện tích bề mặt và dòng. Các màng tương hợp sinh học hoạt hóa bổ thể rất ít. Các màng lọc tổng hợp hiện nay cho phép lọc các chất có TLPT lên đến 30 đến 40 kD.
Về lý thuyết, việc này giúp loại bỏ hầu hết hóa các chất trung gian gây viêm. Tuy nhiên, nồng độ của hầu hết các cytokine huyết tương không thay đổi trong lúc ĐTTTTLT dù tốc độ siêu lọc rất cao. Các màng lọc có điểm cắt cao cho phép lọc các phân tử lên đến 60 kD thúc đẩy thanh thải phân tử lớn liên quan đến nhiễm trùng huyết. Có nhiều loại màng lọc mới đã được phát triển (ví dụ: AN69 được xử lý bề mặt ST, SEPTEX, polymethyl-methacrylate, Oxiris, polymyxin B và CytoSorb) [7].
Loại màng lọc quyết định khả năng loại bỏ chất tan và tính thấm với nước trong lúc ĐTTTTLT. Điểm cắt trọng lượng phân tử, cấu trúc và điện tích màng lọc ảnh hưởng cơ chế đối lưu vận chuyển chất tan xuyên màng cũng như khả năng hấp phụ chất tan. Các chất trung gian gây viêm (IL-6, IL-8, IL-1 và TNF α) có thể được loại bỏ qua cơ chế đối lưu dựa theo trọng lượng phân tử và mức độ gắn kết với protein. Khả năng loại bỏ và hấp phụ các chất tan trọng lượng phân tử lớn trong nhiễm khuẩn huyết và hội chứng đáp ứng viêm toàn thân mang lại nhiều thuận lợi trong phương thức CVVH và CVVHDF [4].
2.3 Phương thức lọc máu
Đời sống quả lọc ngắn hơn khi sử dụng phương thức CVVH so với phương thức CVVHD. Với cùng liều ĐTTTTLT, siêu lọc máu liên quan cô đặc máu do hậu quả của siêu lọc. Trong quả lọc, Hct, tiểu cầu và yếu tố đông máu tăng khả năng đông. CVVHDF kết hợp những thuận lợi của siêu lọc mà lại ít gây cô đặc máu hơn. Thanh thải chất tan có thể đạt được với lưu lượng máu tương đối thấp hơn CVVH mà còn gia tăng đời sống quả lọc [3].
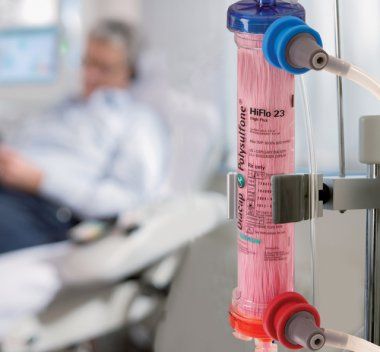
2.4. Tối ưu hóa phân suất lọc FF
Phân suất lọc cao là một trong các yếu tố rút ngắn đời sống quả lọc. Phân suất lọc là tỉ số giữa tốc độ nước được rút ra khỏi cơ thể và lưu lượng huyết tương đến quả lọc. Định nghĩa chính thức của phân suất lọc (FF) là tỷ lệ giữa tốc độ siêu lọc với lưu lượng huyết tương. Lưu lượng huyết tương bằng lưu lượng rút máu x (1 – Hct). Nhằm tối ưu hóa hiệu quả ĐTTTTLT, phân suất lọc giữ mức thấp nhất có thể, không nên vượt quá 20 – 25%. Phân suất lọc cao do Hct sau quả lọc cao thúc đẩy hình thành máu đông và làm giảm chức năng của quả lọc [3],[5].
TÀI LIỆU THAM KHẢO
- Baldwin I. (2007), "Factors affecting circuit patency and filter 'life'", Contrib Nephrol, 156, 178-84.
- Baldwin I., Bellomo R., Koch B. (2004), "Blood flow reductions during continuous renal replacement therapy and circuit life", Intensive Care Med, 30 (11), 2074-9.
- Joannidis M., Oudemans-van Straaten H. M. (2007), "Clinical review: Patency of the circuit in continuous renal replacement therapy", Crit Care, 11 (4), 218.
- Macedo E., Mehta R. L. (2016), "Continuous Dialysis Therapies: Core Curriculum 2016", Am J Kidney Dis, 68 (4), 645-657.
- Michel T., Ksouri H., Schneider A. G. (2018), "Continuous renal replacement therapy: understanding circuit hemodynamics to improve therapy adequacy", Curr Opin Crit Care, 24 (6), 455-462.
- Zhang L., Tanaka A., Zhu G., et al. (2016), "Patterns and Mechanisms of Artificial Kidney Failure during Continuous Renal Replacement Therapy", Blood Purif, 41 (4), 254-63.
- Maiden MJ, R. Bellomo (2019), "Renal Replacement Therapy for Septic Acute Kidney Injury", in Critical Care Nephrology, Ronco C., et al., Editors. pp. 543-548.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.