Bài viết được viết bởi BS Nguyễn Mạnh Hà - Khoa xạ trị - Bệnh viện Đa khoa Quốc tế Vinmec Times City
Ung thư cổ tử cung là loại ung thư phổ biến thứ tư ở phụ nữ trên toàn thế giới, ước tính hàng năm khoảng 5.300.000 ca mắc mới dẫn đến 7,5% tổng số nữ giới tử vong vì ung thư. Khoảng 85% số ca tử vong xảy ra ở các nước đang phát triển do ung thư cổ tử cung hàng năm. Tỷ lệ tử vong cao do cổ tử cung ung thư trên toàn cầu [1] (~52%) có thể được giảm thiểu nhờ hiệu quả chương trình sàng lọc và điều trị.
Những tiến bộ trong công nghệ xạ trị đã giúp ích rất nhiều trong chữa khỏi cho những bệnh nhân ung thư bằng cách cung cấp đủ liều lượng tới khối u và hạn chế liều thấp nhất tới các cấu trúc quan trọng xung quanh [2].
Trong các kỹ thuật xạ trị tương thích 3 chiều (3DCRT-3Dimension Conformal Radiotherapy), người thấy rằng với các trường chiếu trước sau (0 độ)/sau trước (180 độ) hoặc các kế hoạch tạo bởi 4 trường hình hộp (0,90,180,270 độ) cung cấp các liều lượng không cần thiết cho các cơ quan quan trọng lân cận, do đó dẫn đến điều trị liên quan phức tạp sau khi chữa khỏi hoặc tái phát bệnh.
Các kỹ thuật thông thường đã nhường chỗ cho xạ trị điều biến cường độ liều (IMRT-Intensity Modulated Radiotherapy) trong hai thập kỷ qua và gần đây nhất, chúng ta đã thấy sự xuất hiện của kỹ thuật xạ trị điều biến thể tích cung tròn (VMAT-Volume Modulated Arc Thereapy).
- IMRT cung cấp các ưu điểm về việc điều biến liều để cung cấp một liệu đủ lớn tới thể tích điều trị trong khi hạn chế được các liều cao đó tới các cơ quan xung quanh. Tuy nhiên, số lượng MU (monitor unit) phát ra từ kỹ thuật này là rất lớn so với các kỹ thuật thường quy làm tăng nguy cơ ung thư thứ phát [3,4] được gọi là khối u ác tính do bức xạ.
- VMAT có thể hạn chế được các khuyết điểm này của IMRT và phát huy ưu điểm vượt trội về khả năng phân phối liều bằng sử dụng một phần hoặc toàn bộ vòng cung có thể tạo ra số MU nhỏ hơn trong thời gian điều trị ngắn hơn [5].
Để đánh giá phân bố liều từ các kế hoạch VMAT bị ảnh hưởng như thế nào bởi số lượng các vòng cung và năng lượng bức xạ sử dụng chúng tôi đã tiến hành nghiên cứu: “Đánh giá ảnh hưởng của các mức năng lượng và số lượng cung tròn đến phân bố liều trong xạ trị điều biến thể tích cung tròn cho ung thư cổ tử cung”.
Hiện nay, những căn bệnh liên quan đến HPV ngày càng trở nên phổ biến và được cảnh báo nhiều hơn trên các phương tiện truyền thông. Hiểu đúng về HPV sẽ giúp bạn tránh được không ít nguy cơ dẫn đến ung thư các bộ phận sinh dục.
Bài dịch từ: webmd.com
1. Đối tượng và phương pháp nghiên cứu
1.1 Đối tượng
Từ tháng 10/2018 đến tháng 5/2020, 15 bệnh nhân ung thư biểu mô cổ tử cung được xạ trị tại Khoa Xạ trị - Bệnh viện Đa khoa Quốc tế Vinmec Times City. Trong số 15 bệnh nhân có độ tuổi trung bình là 43.5±5.9.
Trong đó có 07 Bệnh nhân giai đoạn (III) và 08 Bệnh nhân giai đoạn (II) theo phân loại giai đoạn của NCCN (2019). Các kế hoạch VMAT với năng lượng 6 MV và 15 MV sử dụng một cung (SA-Single Arc), hai cung (DA- Dual Arc) và 3 cung (TA-Triple Arc) đã được lập cho mỗi bệnh nhân.
1.2 Phương pháp nghiên cứu
1.2.1 Quy trình nghiên cứu
Tất cả bệnh nhân (BN) được cố định bằng cách sử dụng mặt nạ kèm vack log tiểu khung (hãng Civco, Mỹ) để đảm bảo phần từ bụng đến xương đùi được giữ cố định và ổn định trong suốt đợt điều trị xạ trị.
Hình ảnh chụp cắt lớp (CT) với độ dày 2,5 mm thu được trên máy chụp CT mô phỏng 16 lát GE optimal 580 (GE, Mỹ). BN đã được hướng dẫn và thực hiện quy trình chuẩn bị bàng quang trước khi chụp CT mô phỏng và điều trị.
Theo đó, BN sẽ làm rỗng bàng quang và được uống một lượng nước 500-1000ml nhất định tùy thuộc vào từng BN, sau đó được đợi trong 1 khoảng thời gian cố định từ 45 phút trở lên để đảm bảo bàng quang đã được làm đầy.
Bác sĩ có kinh nghiệm về chẩn đoán hình ảnh xác định chính xác các vùng cơ quan nguy cơ (Ogan at Risk- OAR) cho tất cả các bệnh nhân cùng với một kỹ sư vật lý thể thiết kế tính toán liều lượng cho kế hoạch xạ trị. OAR bao gồm: Bàng quang (Bladder), trực tràng (rectum), túi ruột (bowel bag), chỏm xương đùi 2 bên (Femur_Lt, RT), tủy sống (Spinal Cord), Xương chậu (Illiac bone), phần mô bình thường (Body-PTV).
PTV được xác định dựa trên các hướng dẫn được đề xuất bởi Ủy ban Quốc tế về Bức xạ và Đơn vị ICRU 50 và ICRU 62 [6,7] và các protocol xạ trị ung thư RTOG (Lim và cộng sự, 2011). PTV được chỉ định liều 50.4Gy/28 phân liều và cấp cho bệnh nhân mỗi ngày một phân liều, 5 phân liều/tuần.
Tất cả các kế hoạch VMAT (SA6MV, DA6MV, TA6MV, SA15MV, DA15MV, TA15MV) đều được hiệu chỉnh mức normalization hay chuẩn hóa ở cùng một tiêu chuẩn để việc so sánh được chính xác như sau: 100% liều lượng chỉ định (70Gy) bao phủ được đến 95% thể tích mục tiêu.
Về OAR: Liều tới các cơ quan nguy cấp cần được giảm thiểu tối đa trong phạm vi hợp lý trong bảng 1 và không ảnh hưởng tới mục tiêu điều trị.

1.2.2 Kế hoạch VMAT
Các kế hoạch VMAT (SA, DA, TA) cho mỗi BN được chúng tôi thiết lập trên phần mềm lập kế hoạch Eclipse phiên bản 13.0 của hãng Varian (Mỹ). Các kế hoạch dùng các cung gantry đồng phẳng, dùng mức năng lượng 6 MV, suất liều 600 MU/phút, thuật toán AAA để tính toán tối ưu hóa.
Kế hoạch SA gồm một cung gantry được thiết kế quay từ 179 độ tới 181 độ. Kế hoạch DA gồm một cung gantry được thiết kế quay từ 179 độ tới 181 độ (ngược chiều kim đồng hồ) và một cung ngược lại (cùng chiều kim đồng hồ) với hai góc collimator 10 và 80 độ, dựa theo nghiên cứu trước đó của nhóm chúng tôi về ảnh hưởng của góc collimator tới phân bố liều trong kế hoạch VMAT [8].
Kế hoạch TA cũng được thiết kế tương tự, gồm 1 cung gantry quay từ 179 đến 181 độ với góc collimator 10 độ và 2 cung còn lại có góc cùng là collimator 80 độ, góc gantry từ 179 đến 181 độ và ngược lại với lý do là thể tích PTV có độ dài lớn có thể chia một cung thành hai cung với kích thước trường chiếu nhỏ hơn để giảm khoảng cách dịch chuyển giữa các lá MLC và giảm sai số giữa các lá MLC. Các kế hoạch SA, DA, TA sau đó được thiết lập với mức năng lượng 15MV cho mỗi BN, các thông số thiết kế giống như đối với mức 6MV.
1.2.3 Đánh giá và so sánh kế hoạch
Chỉ số chất lượng kế hoạch của các kế hoạch VMAT được phân tích bằng biểu đồ liều-thể tích (DVH). Biểu đồ DVH đại diện cho toàn bộ thông tin về liều lượng trong một đường cong hai chiều và được tham khảo dựa trên hướng dẫn của ủy ban quốc tế về đơn vị bức xạ (ICRU83) [9].
Độ bao phủ của thể tích lập kế hoạch (PTV) và liều trung bình tới các cơ quan nguy cơ (OAR) có nghĩa là (Dmean) và liều tối đa (Dmax), chỉ số sự phù hợp (CI) [10] và chỉ số đồng nhất (HI) được phân tích cho tất cả các kế hoạch. Đối với tất cả bệnh nhân, tổng số MUs trên mỗi phân liều và thời gian phát tia cho mỗi kế hoạch đã được ghi nhận so sánh.
- Chỉ số phù hợp (CI) được định nghĩa như sau: CI = TVRI/TV
Trong đó: TVRI = thể tích mục tiêu được bao phủ bởi liều tham khảo (thể tích PTV nhận liều tham khảo trong báo cáo là 98%). TV = thể tích mục tiêu. Giá trị lý tưởng là 1. Chỉ số phù hợp (CI) thể hiện mức độ phù hợp của đường đồng liều với hình dạng và kích thước của mục tiêu.
- Chỉ số đồng nhất (HI) được định nghĩa như sau: HI = (D2% - D98%)/D50%
Trong đó: D2% là liều tới 2% thể tích PTV; D98% là liều tới 98% thể tích PTV; D50% là liều tới 50% thể tích PTV. Chỉ số đồng nhất (HI) mô tả tính đồng nhất của liều trong một khối lượng mục tiêu và được tính trực tiếp từ số liệu thống kê của biểu đồ khối lượng liều lượng. Chỉ số HI càng gần 0 càng lý tưởng (ICRU83).
1.2.4 Phân tích thống kê
So sánh thống kê độ bao phủ liều PTV và liều lượng của OAR giữa các kế hoạch VMAT được thực hiện bằng cách sử dụng phân tích dữ liệu thống kê bằng hệ thống SPSS v15.5. Kết quả được báo cáo là trung bình và độ lệch chuẩn. Giá trị ý nghĩa thống kê được lưu giữ tại p <0,05, các giá trị p >0.05 không có ý nghĩa (NS-nonsignificant).
2. Kết quả thực tế


*{Giá trị trong bảng = Giá trị trung bình ± Độ lệch chuẩn; giá trị p: NS = Nonsignificant = không có ý nghĩa (>0.05)}
Tất cả các kế hoạch được đánh giá đạt các yêu cầu về liều giới hạn và phân bố liều tới PTV, đủ điều kiện đem điều trị trên thực tế trước khi được đem so sánh với nhau. Mức độ bao phủ liều tới PTV đã được so sánh trong tất cả các mức năng lượng và số cung (bảng 2).
Thể tích V98 cho kế hoạch TA6MV(97.93±0.35) tốt hơn DA6MV(97.84±0.34), SA6MV(97.63±0.23); kế hoạch TA15MV(97.98±0.39) tốt hơn DA15MV(97.87±0.34), SA15MV(97.68±0.3) (p <0,05).
Liều tới 2% (D2) của PTV trong các kế hoạch SA6MV(56.31±1.27) và SA15MV(56.07±1.42) là lớn nhất (p<0.05). Kế hoạch TA6MV có CI (0.979), HI (0.112) tốt hơn CI (0.978) và HI (0.117) của DA6MV và SA6MV(CI=0.976; HI=0.132), tương tự CI (0.979), HI (0.111) đối với TA15MV tốt hơn DA15MV (CI=0.978; HI=0.117) và SA15MV(CI=0.976; HI=0.127), p<0,05).
Trên hình 1 cho thấy rõ phân bố liều V98, D2, CI, HI tới PTV giữa các kế hoạch TA6MV và TA15MV; DA6MV và DA15MV khác nhau không đáng kể (p>0.05).




Bảng 2 cho kết quả về thời gian cấp liều và số MUs trong các kế hoạch SA lần lượt ít hơn so với các kế hoạch DA và TA ở cả hai mức năng lượng 6MV và 15MV (p<0.05).
Các thông số được đánh giá cho thấy liều OAR giảm đáng kể (bảng 3). Liều trung bình (Dmean) và Liều cực đại (Dmax), thể tích nhận liều 40Gy (V40Gy) tới túi ruột (Bowel bag) của kế hoạch TA là tốt hơn so với các kế hoạch SA, DA ở cả hai mức năng lượng 6MV và 15MV (p<0.05).
Liều trung bình tới bàng quang cũng tốt hơn ở các kế hoạch TA so với các kết hoạch SA và DA ở cả hai mức 6MV và 15MV (p<0.05). Ở mức 6MV, Liều trung bình tới trực tràng ở các kế hoạch TA6MV(41.48±3.22) tốt hơn so với DA6MV(41.66±3.22), SA6MV(42.17±3.11) (p<0.05).
Liều tới thể tích mô lành (Body-PTV) không có nhiều sự khác biệt giữa các kế hoạch trong cùng 1 mức năng lượng 6MV (SA, DA, TA) hoặc 15 MV (SA, DA, TA) (p>0.05); khi so sánh giữa các mức năng lượng với nhau cho thấy TA15MV và DA15MV có liều Dmean (9.3; 9.5), V5Gy (46.68; 46.64) thấp hơn so với Dmean (10.2; 10.0), V5Gy (47.2; 47.0) của TA6MV và DA6MV (p<0.05).



Trên bảng 4 cho thấy kết quả phân bố liều tới chỏm xương đùi hai bên không thay đổi ở các kế hoạch (p>0.05). Liều trung bình, liều cực đại tới xương chậu trong kế hoạch TA tốt hơn DA và SA ở cả hai mức 6MV và 15MV (p<0.05). Tại năng lượng 15MV liều V10Gy trong kế hoạch TA15MV (93.01±4.11, p<0.05) thấp hơn trong các kế hoạch khác. Tại mức 6M liều V40Gy trong kế hoạch TA6MV (15.4±5.35) là thấp nhất (p<0.05).
3. Bàn luận
Kết quả trên bảng 2 và hình 1 cho thấy các kế hoạch TA đều có phân bố liều tới PTV tốt hơn so với SA, DA ở cả 2 mức năng lượng 6MV và 15MV (p<0.05). Kết quả được giải thích là do TA sử dụng 3 cung tròn nhiều hơn SA (1 cung) và DA (2 cung) nên khả năng điều biến liều lượng và tối ưu tốt hơn các kế hoạch khác. So sánh ảnh hưởng của mức năng lượng trên các kế hoạch DA6MV với DA15MV và TA6MV với TA15MV (hình 1) cho thấy kết quả không có sự khác biệt nhiều (p>0.05), kết quả này giống với kết quả của Sternick và cộng sự [11] trong nghiên cứu về ảnh hưởng của năng lượng từ 4-18MV trong IMRT tiền liệt tuyến.
Báo cáo của chúng tôi cũng cho kết quả tương tự với tác giả Lalit Kumar [12] trong so sánh ảnh hưởng các mức 6, 10, 15MV trong ung thư cổ tử cung và tác giả Girigesh Yadav [13] khi so sánh ảnh hưởng của 6, 10, 15MV trong các kế hoạch SA, DA cho ung thư tử cung.
Cũng trong bảng 2 thời gian cấp liều và số MUs trong các kế hoạch SA lần lượt ít hơn so với các kế hoạch DA và TA ở cả hai mức năng lượng 6MV và 15MV (p<0.05) được giải thích là do kế hoạch SA sử dụng 1 cung nên thời gian để cấp liều trong 1 cung đó ít hơn so với 2 cung của DA và 3 cung của TA.
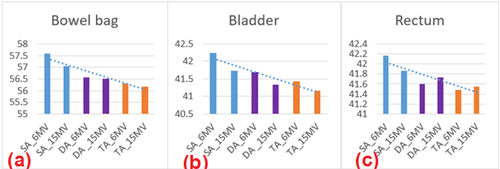
Đồng thời Do số MU phát ra từ 1 cung cũng nhỏ hơn so với các kế hoạch nhiều cung. Kết quả này giống với nghiên cứu của Lalit Kumar [12] về số MUs. Mặt khác số MUs trong TA15MV ít hơn TA6MV là do mức năng lượng 15MV có độ sâu phần trăm lớn hơn với 6MV nên số MU phát ra để đạt được liều cần thiết tại cùng một độ sâu của 15MV là ít hơn. Số MUs được biểu diễn rõ hơn qua biểu đồ trong hình 3c.
Ở bảng 3 và hình 2 cho thấy liều tới các cơ quan nguy cấp như: Dmean, Dmax và V40Gy tới Túi ruột và Dmean tới bàng quang, Dmean tới trực tràng của kế hoạch TA là tốt hơn so với các kế hoạch SA, DA ở cả hai mức năng lượng 6MV và 15MV (p<0.05) được giải thích là khả năng điều biến trong kế hoạch TA tốt hơn nhờ số cung lớn nên số điểm điều biến lớn hơn.
Liều tới thể tích mô lành (bảng 2, hình 3a) khi so sánh các mức năng lượng trong kế hoạch TA và DA, liều Dmean, V5Gy của mức 15MV tôt hơn so với 6MV (p<0.05), được giải thích là do số MU trong các kế hoạch MU lớn hơn, nên phần liều thấp xung quanh thể tích PTV sẽ nhiều hơn, điều này phù hợp với các nghiên cứu đã được trình bày [14,15].

Trên bảng 4 và hình 3b cho thấy các giá trị Dmean, Dmax tới xương chậu trong kế hoạch TA tốt hơn DA và SA ở cả hai mức 6MV và 15MV (p<0.05). Tại năng lượng 15MV liều V10Gy trong kế hoạch TA15MV (93.01±4.11, p<0.05) thấp hơn trong các kế hoạch khác.
Tại mức 6M liều V40Gy trong kế hoạch TA6MV (15.4±5.35) là thấp nhất (p<0.05). V10Gy trong kế hoạch TA15MV tốt hơn, và V40Gy trong TA6MV thấp nhất, được giải thích giống như phần trên do mức năng lượng 15MV độ sâu phần trăm lớn hơn với 6MV cần ít hơn MU để cấp liều tới cùng một độ sâu nên phần liều cao tập trung gần PTV hơn (V40Gy) trong khi phần liều thấp V10Gy xung quanh PTV lại ít hơn so với mức 6MV.
4. Kết luận
Nghiên cứu cho thấy các kế hoạch sử dụng năng lượng cao 15MV không tốt hơn so với 6MV trong phân bố liều tới PTV và tới các cơ quan nguy cấp. Kế hoạch TA6MV là một lựa chọn tốt trong điều trị ung thư cổ tử cung vì liều bao phủ, độ đồng nhất và phù hợp tới mục tiêu điều trị cao hơn đồng thời bảo vệ các cơ quan nguy cấp tốt hơn.
Tài liệu tham khảo:
[1]. World Health Organization (WHO) Reports on Cervical Cancers. HPV and Cervical Cancer in the World 2007, vol. 25(Suppl. 1). 2007.
[2]. Gupta D, Shukla P et al. Comparitive study of efficacy, tolerability of four field box technique vs. two field anterior posterior technique in locally advanced carcinoma cervix. Cancer Biol Ther 2009.
[3]. Kry SF, Salehpour M, et al. The calculated risk of fatal secondary malignancies from IMRT. Int J Radiat Oncol Biol Phys2005.
[4]. Kry, Kry SF, Followill D, et al. Uncertainty of calculated risk estimates for secondary malignancies after radiotherapy. Int J Radiat Oncol Biol Phys 2007.
[5]. Cozzi L, et al. A treatment planning study comparing volumetric arc modulation with RapidArc and fixed field IMRT for cervix uteri radiotherapy. Radiother Oncol2008.
[6]. ICRU Report 50. Prescribing, Recording, and Reporting Photon Beam Therapy (1993).
[7] ICRU Report 62. Prescribing, Recording, and Reporting Photon Beam Therapy (1999).
[8]. Nguyen Dinh Long, Tran Ba Bach và cộng sự: Ảnh hưởng của góc Collimator tới phân bố liều trong xạ trị cung tròn cho NPC, tạp chí Ung thư học VN số 5 (2017).
[9] ICRU Report 83. Prescribing, Recording, and Reporting Photon-Beam IMRT (2010).
[10]. Van’t Riet A, (1997): A conformation number to quantify the degree of conformality in brachytherapy and external beam irradiation. Int J Radiat Oncol Biol Phys, 37, 731-6.
[11]. Sternick ES, et al. IMRT: What photon energy isbest? Medical Physics; 1997. p. 418-9.
[12]. Lalit Kumar et al. The dosimetric impact of different photon beam energy on RapidArc radiotherapy planning for cervix carcinoma, Journal of Medical Physics (2015).
[13]. Girigesh Yadav el at. Dosimetric influence of photon beam energy and number of arcs on VMAT in carcinoma cervix: A planning study, Published by Elsevier (2016).
[14] D’Souza WD, Rosen II. Nontumor integral dose variation in conventional radiotherapy treatment planning, Med Phys 2003.
[15]. Pirzkall A, et al. The effect of beam energy and number of fields on photon-based
IMRT for deep-seated targets. Int J Radiat Oncol Biol Phys 2002.