Bài viết được viết bởi ThS, BS. Mai Viễn Phương, Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Trí tuệ nhân tạo có khả năng được áp dụng trong quá trình nội soi đại tràng để tự động phát hiện ra các polyp đại trực tràng và phân biệt giữa polyp ung thư và không phải ung thư, với khả năng cải thiện tỷ lệ phát hiện u tuyến, tỷ lệ này thay đổi rộng giữa các bác sĩ nội soi khi thực hiện kiểm tra nội soi đại tràng.
1. Tổng quan về trí tuệ nhân tạo AI
Trí tuệ nhân tạo (AI) cho phép máy móc cung cấp giá trị đột phá trong một số ngành và ứng dụng. Các ứng dụng của kỹ thuật AI, đặc biệt là học máy (machine learning) và gần đây là học sâu (deep learning), đang phát triển trong khoa tiêu hóa. Chẩn đoán có sự hỗ trợ của máy tính cho nội soi đường tiêu hóa trên ngày càng được chú ý để xác định tự động và chính xác chứng loạn sản trong thực quản Barrett, cũng như để phát hiện ung thư dạ dày sớm (GCs), do đó ngăn ngừa các khối u ác tính ở thực quản và dạ dày. Bên cạnh đó, công nghệ mạng lưới thần kinh phức tạp có thể đánh giá chính xác tình trạng nhiễm vi khuẩn Helicobacter pylori (H. pylori) trong quá trình nội soi tiêu chuẩn mà không cần sinh thiết, do đó, giảm nguy cơ ung thư dạ dày. Trí tuệ nhân tạo có khả năng được áp dụng trong quá trình nội soi đại tràng để tự động phát hiện ra các polyp đại trực tràng và phân biệt giữa polyp ung thư và không phải ung thư, với khả năng cải thiện tỷ lệ phát hiện u tuyến, tỷ lệ này thay đổi rộng giữa các bác sĩ nội soi khi thực hiện kiểm tra nội soi đại tràng. Ngoài ra, AI cho phép thiết lập tính khả thi của thủ thuật cắt bỏ polyp qua nội soi các tổn thương polyp đại tràng có kích thước lớn dựa trên các đặc điểm bề mặt và thay đổi vi mạch máu
2. Giới thiệu về thuật toán học máy và học sâu
Học máy (ML) và học sâu (DL) có thể được coi là các lĩnh vực con của trí tuệ nhân tạo. ML là một dạng trí tuệ nhân tạo có thể hỗ trợ quá trình ra quyết định, cho phép cải tiến các thuật toán được áp dụng mà không cần lập trình, bao gồm cả kiểm tra dữ liệu và triển khai các mô hình mô tả và dự đoán (Hình 1).
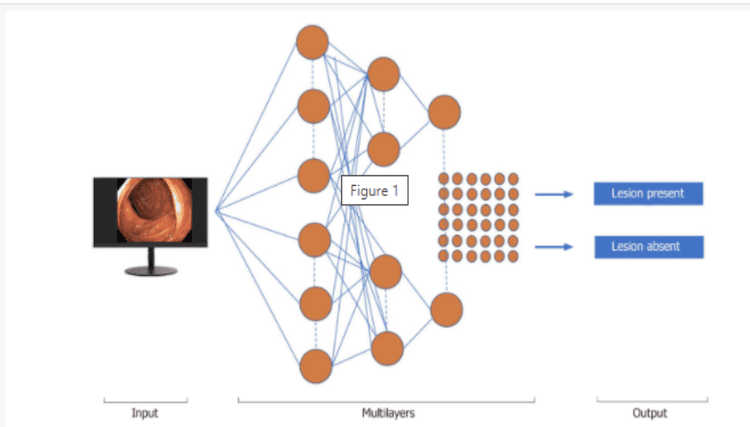
Thuật toán học máy (Machine learning – ML) được phân biệt thành các phương pháp có giám sát và không được giám sát. Một ví dụ của công nghệ học máy được giám sát, mạng nơ-ron nhân tạo (ANN), phản ánh chức năng sơ đồ của não. Mỗi nơron là một đơn vị tính toán và tất cả các nơron được kết nối để tạo ra một mạng. Các thuật toán học máy và mạng nơ-ron phức tạp (CNN) đã được tạo ra để huấn luyện phần mềm phân biệt vùng bình thường với vùng bất thường trong lòng ruột. Để phát hiện polyp, công nghệ học máy sử dụng một số đặc điểm cố định, chẳng hạn như kích thước, hình dạng và các kiểu niêm mạc của polyp.
3. Trí tuệ nhân tạo, thực quản Barrett và ung thư thực quản
Barrett thực quản (BE) được đặc trưng bởi sự biến đổi bất thường (tăng sản) của các tế bào niêm mạc, lót phần dưới của thực quản, từ biểu mô vảy phân tầng bình thường thành biểu mô hình cột và liên kết với các tế bào hình cốc xen kẽ. Tình trạng này đại diện cho một yếu tố nguy cơ của ung thư biểu mô tuyến thực quản (EAC) mà tiên lượng nghiêm trọng nhất liên quan đến chẩn đoán muộn. Hơn nữa, 93% bệnh nhân có thể thuyên giảm bệnh hoàn toàn sau khi điều trị và theo dõi thường xuyên trong 10 năm. Các kỹ thuật đầy hứa hẹn để quản lý Barrett thực quản với khả năng làm giảm nguy cơ ung thư bằng cách chẩn đoán chính xác chứng loạn sản, đang được phát triển.
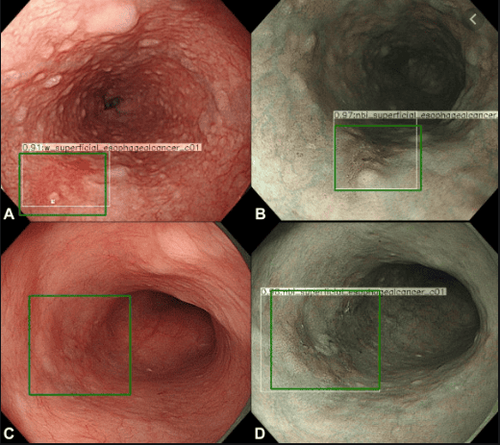
Vẫn dựa trên hệ thống mạng nơ-ron phức tạp CNN và kiến trúc ResNet với DeepLab V.3 +, một mạng bộ mã hóa - giải mã hiện đại đã được điều chỉnh lại. Để truyền Livestream nội soi sang hệ thống AI của chúng tôi, một thẻ chụp (Avermedia, Đài Loan) để truyền hình ảnh đã được tích hợp vào màn hình nội soi và hệ thống AI đã được đào tạo bằng cách sử dụng 129 hình ảnh nội soi. Tất cả các kết quả hình ảnh AI đã được xác nhận bằng cách kiểm tra bệnh lý của các mẫu cắt bỏ của ung thư thực quản cũng như sinh thiết kẹp (tức là Barrett thực quản đơn thuần). Hệ thống AI cho thấy điểm hiệu suất cao trong công dụng phân loại tổn thương với độ nhạy và độ đặc hiệu lần lượt là 83,7% và 100%.
4. Vai trò của mạng nơ-ron phức tạp CNN trong chẩn đoán bệnh lý tiêu hóa
Mạng nơ-ron phức tạp CNN cũng được sử dụng bởi Horie và cộng sự, thu thập hồi cứu 8428 hình ảnh đào tạo từ bệnh ung thư thực quản của 384 bệnh nhân thông qua mạng nơ-ron phức tạp CNN. CNN đã mất 27 giây để phân tích 1118 hình ảnh thử nghiệm và phát hiện chính xác các trường hợp ung thư thực quản với độ nhạy 98%. Hệ thống mạng nơ-ron phức tạp phát hiện cứ 7 tổn thương ung thư nhỏ có kích thước dưới 10 mm. Hệ thống này tạo điều kiện phát hiện bệnh ác tính sớm và nhanh chóng dẫn đến tiên lượng tốt hơn cho những bệnh nhân này.
AI có thể hỗ trợ các bác sĩ nội soi làm sinh thiết mục tiêu với độ chính xác cao, tiết kiệm công việc / lấy mẫu ngẫu nhiên tốn nhiều thời gian, với độ nhạy thấp (64%) để phát hiện dị sản. Một thử nghiệm quốc tế, ngẫu nhiên, chéo, so sánh nội soi ánh sáng trắng độ nét cao (HD-WLE) và NBI để phát hiện IM và bệnh ác tính ở 123 bệnh nhân bị BE (kích thước chu vi trung bình và kích thước tối đa, tương ứng là 1,8 và 3,6 cm) .
5. Nội soi vi mô (ở mức độ tế bào) độ phân giải cao (HRME)
Nội soi vi mô (ở mức độ tế bào) độ phân giải cao (HRME) đã cho thấy tiềm năng tăng cường phát hiện SCC thực quản trong quá trình sàng lọc. Một thuật toán phân tích thời gian thực, tự động đã được phát triển và đánh giá bằng cách sử dụng các bài kiểm tra đào tạo và hình ảnh xác thực thu được từ một nghiên cứu in-vivo trước đó bao gồm 177 đối tượng tham gia cho các chương trình sàng lọc/ giám sát. Trong một phân tích hậu kỳ, thuật toán đã nhận ra các khối u ác tính với độ nhạy 95% và độ đặc hiệu 91%, trong bộ dữ liệu xác nhận, trong khi 84% và 95% trong nghiên cứu ban đầu. Do đó, công nghệ này có thể được áp dụng trong các cơ sở có người vận hành ít chuyên môn hơn trong việc giải thích hình ảnh HRME.

6. Trí tuệ nhân tạo và ung thư dạ dày
Ung thư dạ dày (GC) đứng hàng thứ ba trong nguyên nhân chính gây tử vong do bệnh lý ác tính trên toàn thế giới, và nội soi dạ dày tá tràng (EGD) được coi là công cụ chẩn đoán tốt nhất cho ung thư ở giai đoạn đầu. Việc điều trị u dạ dày phụ thuộc vào độ sâu của sự xâm lấn dưới niêm mạc; thực sự, đối với các khối u trong niêm mạc đã biệt hóa (M) hoặc những khối u xâm lấn vào lớp dưới niêm mạc nông (≤ 500 lm: SM1), kỹ thuật cắt niêm mạc EMR hoặc cắt bóc tách dưới niêm mạc ESD được thực hiện để cắt bỏ tổn thương, trong khi những khối u có xâm lấn sâu dưới niêm mạc (> 500 lm: SM2) nên được điều trị bằng phẫu thuật để tránh nguy cơ tiềm ẩn xâm lấn và di căn tại chỗ. Nội soi phóng đại kết hợp với NBI hoặc FICE (tăng cường màu sắc linh hoạt của hình ảnh quang phổ) hữu ích về mặt lâm sàng trong việc phân biệt ác tính dạ dày với các vùng không ác tính. Tuy nhiên, chẩn đoán quang học này hoàn toàn phụ thuộc vào chuyên môn và kinh nghiệm của người thực hiện, điều này ngăn cản việc sử dụng chung trong thực hành lâm sàng.
Miyaki và cộng sự, đã phát triển phần mềm cho phép đánh giá định lượng GC niêm mạc trên hình ảnh nội soi tiêu hóa phóng đại thu được bằng FICE. Họ đã thông qua một bộ khung đặc điểm có các bộ mô tả biến đổi tính năng bất biến ở quy mô được lấy mẫu dày đặc để phóng đại hình ảnh FICE của 46 trường hợp ung thư dạ dày trong niêm mạc sau đó so sánh với các phát hiện mô học. Hệ thống CAD cho phép độ chính xác phát hiện là 86%, độ nhạy và độ đặc hiệu là 85% và 87% đối với chẩn đoán ung thư.
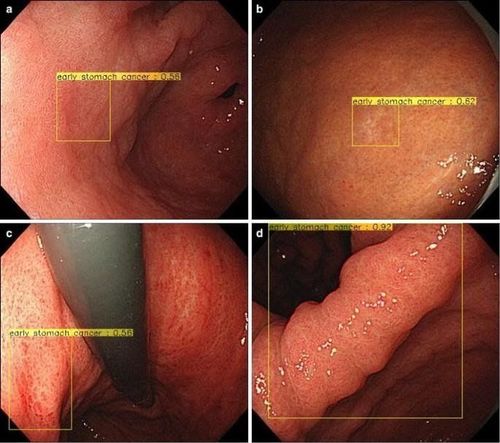
7. Vai trò của AI trong dự đoán tiên lượng của bệnh nhân mắc ung thư dạ dày
AI có thể hỗ trợ các bác sĩ dự đoán tiên lượng của bệnh nhân mắc ung thư dạ dày. Một số thử nghiệm lâm sàng quan trọng đánh giá các chiến lược bổ trợ của ung thư dạ dày tiến triển cao đã được sản xuất trong thập kỷ qua, nhưng liệu pháp phù hợp nhất cho ung thư dạ dày cho đến nay vẫn chưa chắc chắn. Bên cạnh đó, hai nghiên cứu cảnh quan phân tử đương đại đã chứng minh sự hiện diện của các phân nhóm ung thư dạ dày phân tử khác nhau. Một mô hình dựa trên thuật toán học sâu (mạng tái phát sinh tồn, SRN) được phát triển để dự đoán các biến cố sống sót cho tổng số 1190 bệnh nhân ung thư dạ dày, dựa trên dữ liệu lâm sàng/ bệnh lý cũng như phác đồ điều trị, dự đoán kết quả tại từng thời điểm trong thời gian 5 thời gian giám sát năm. SRN chỉ ra rằng loại phụ trung mô của ung thư dạ dày nên kích thích một chiến lược điều trị sau phẫu thuật phù hợp do hậu quả của tỷ lệ tái phát rất lớn.
8. Trí tuệ nhân tạo AI trong việc xác định nhiễm khuẩn Helicobacter pylori
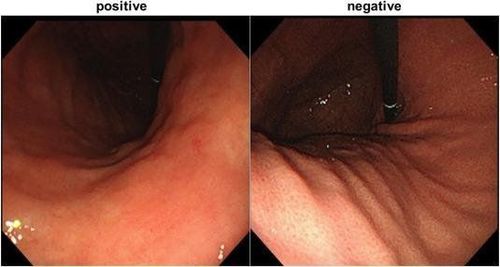
Helicobacter pylori (H. pylori) nhiễm vào tế bào biểu mô dạ dày và có liên quan đến rối loạn tiêu hóa chức năng, loét dạ dày tá tràng, teo niêm mạc, chuyển sản ruột và ung thư dạ dày. Viêm dạ dày mãn tính liên quan đến H. pylori cũng có thể làm tăng nguy cơ mắc ung thư dạ dày. Công nghệ CNN có thể đánh giá chính xác tình trạng nhiễm H. pylori trong quá trình nội soi thông thường mà không cần sinh thiết. Trong một nghiên cứu thử nghiệm của Zheng và cộng sự , các tác giả đã đưa ra Hệ thống hỗ trợ quyết định có sự hỗ trợ của máy tính sử dụng CNN để ước tính nhiễm H. pylori dựa trên hình ảnh nội soi. Từ 1959 bệnh nhân, 77% được chỉ định vào nhóm xác nhận (1507 bệnh nhân; 11729 hình ảnh dạ dày) và 56% trong số họ bị nhiễm H. pylori (847), trong khi 23% được chọn vào nhóm xác nhận (452) và 69% bệnh nhân bị nhiễm H. pylori (310; tổng số 3755 hình ảnh).
9. Trí tuệ nhân tạo AI cho vấn đề chẩn đoán polyp và ung thư đại tràng
Ung thư đại trực tràng (CRC) là bệnh ác tính thường gặp thứ ba ở nam và thứ hai ở nữ, và là nguyên nhân phổ biến thứ tư gây ra tử vong do ung thư. Nghiên cứu Quốc gia về Polyp đã đăng ký rằng 70% -90% CRC có thể được ngăn ngừa bằng cách theo dõi nội soi thường quy và cắt bỏ polyp, nhưng 7% -9% CRC có thể xảy ra bất chấp các biện pháp này.
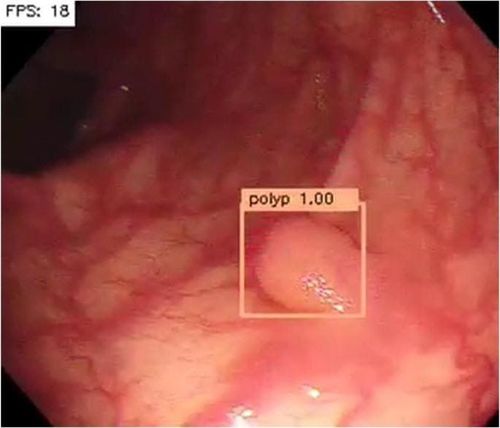
Khoảng 85% “ung thư khoảng cách” là do các polyp bị bỏ sót hoặc cắt bỏ không đầy đủ các polyp. U tuyến là tổn thương tiền ung thư phổ biến nhất trên khắp đại tràng. ADR đo khả năng của bác sĩ nội soi để xác định các u tuyến. ADR dao động từ 7% –53% trong số các bác sĩ nội soi thực hiện tùy thuộc vào trình độ của họ, kỹ thuật cắt bỏ nội soi, thời gian rút, chất lượng chuẩn bị ruột và các yếu tố quyết định phụ thuộc vào quy trình khác.
10. Một số cải tiến nội soi đã được thúc đẩy để tăng ADR
Một đánh giá bao gồm 5 nghiên cứu về ảnh hưởng của ống soi đại tràng độ phân giải cao đối với ADR cho thấy các kết quả trái ngược nhau; một nghiên cứu kết luận rằng ADR được nâng lên dành riêng cho các bác sĩ nội soi với ADR thấp hơn 20% .
Một nghiên cứu tiền cứu trên 55 bệnh nhân đã sử dụng nguyên mẫu của một phần mềm phát hiện polyp tự động mới (APDS) để phát hiện polyp dựa trên hình ảnh tự động và với tỷ lệ phát hiện polyp tổng thể trong thời gian thực là 75%. Kích thước polyp nhỏ hơn và hình thái polyp phẳng có liên quan đến việc APDS không phát hiện đủ polyp.
11. Trí tuệ nhân tạo giúp phân biệt giữa u tuyến và polyp tăng sản
Ngoài máy móc CADe, hệ thống CADx còn được sử dụng để phân biệt giữa u tuyến và polyp tăng sản.
Byrne và cộng sự đã đề xuất việc sử dụng phân tích hình ảnh trên máy tính để giảm bớt sự thay đổi trong phát hiện nội soi và dự đoán mô học. Mô hình AI này đã được đào tạo bằng cách sử dụng video nội soi và có thể phân biệt giữa các u tuyến nhỏ và polyp tăng sản với độ chính xác cao. Ngoài ra, nó dự đoán mô học với độ chính xác 94%, độ nhạy 98%, độ đặc hiệu 83%, giá trị dự đoán âm tính và dương tính lần lượt là 97% và 90%.
Hotta và cộng sự nhằm xác nhận hiệu quả của hệ thống nội soi (EC) -CAD trong việc chẩn đoán tổn thương đại trực tràng ác tính hoặc không ác tính, bằng cách so sánh khả năng chẩn đoán giữa các nhà nội soi chuyên nghiệp và không chuyên gia, bằng cách sử dụng các xét nghiệm dựa trên web. Một xét nghiệm xác nhận đã được thực hiện bằng cách sử dụng hình ảnh nội soi của 100 tổn thương đại trực tràng nhỏ (<10 mm). Độ chính xác và độ nhạy chẩn đoán của EB-01 và không chuyên đối với hình ảnh nội soi nhuộm màu là 98,0% so với 69,0%, cho thấy độ chính xác và độ nhạy chẩn đoán cao hơn đáng kể đối với các bác sĩ nội soi không chuyên khi chẩn đoán các tổn thương đại trực tràng nhỏ.
Thuật toán học sâu còn giúp phân biệt những bệnh nhân có đáp ứng hoàn toàn với hóa trị liệu bổ trợ cho ung thư trực tràng tiến triển tại chỗ với độ chính xác 80%. Hỗ trợ công nghệ này có thể cho phép chọn những bệnh nhân đặc biệt có lợi cho điều trị bảo tồn hơn là phẫu thuật cắt bỏ hoàn toàn. Đây là nghiên cứu đầu tiên sử dụng Thuật toán học sâu để dự đoán đáp ứng bệnh lý toàn bộ sau khi hóa trị liệu bổ trợ trong ung thư trực tràng tiến triển tại chỗ.

12. Một số giới hạn của trí tuệ nhân tạo
Trí tuệ nhân tạo AI có thể đại diện cho một phương pháp chẩn đoán cần thiết cho các bác sĩ nội soi và bác sĩ tiêu hóa để điều trị bệnh nhân phù hợp và dự đoán kết quả lâm sàng của họ. Trí tuệ nhân tạo dường như đặc biệt có giá trị trong nội soi tiêu hóa, để cải thiện việc phát hiện các tổn thương tiền ác tính và ác tính, hoặc tổn thương viêm, xuất huyết tiêu hóa và các bệnh lý tuyến tụy. Tuy nhiên, những hạn chế hiện tại của Trí tuệ nhân tạo bao gồm thiếu bộ dữ liệu chất lượng cao để phát triển thuật toán học máy ML. Hơn nữa, một bằng chứng quan trọng được sử dụng để xây dựng các thuật toán học máy chỉ đến từ các nghiên cứu tiền lâm sàng. Không thể loại trừ các thành kiến lựa chọn tiềm năng trong những trường hợp như vậy. Trong bối cảnh này, cần phải xác nhận chặt chẽ hiệu suất của AI trước khi sử dụng nó trong thực hành lâm sàng hàng ngày. Một thước đo thực sự về độ chính xác của AI, nên bao gồm như một hiệu ứng phụ trong các hiệu suất quá mức và sai lệch phổ. Overfitting (vấn đề quá phù hợp) xảy ra khi một mô hình học tập tự điều chỉnh quá nhiều trên tập dữ liệu huấn luyện và các dự đoán không được khái quát hóa tốt cho tập dữ liệu mới. Hiệu ứng này mâu thuẫn rõ ràng với nguyên tắc giải quyết vấn đề của Occam’s razor, trong đó nói rằng các lý thuyết đơn giản hơn có chất lượng dự đoán cao hơn. Trong trường hợp xấu nhất của ứng dụng thuật toán AI, có thể xảy ra tình trạng thiếu trang bị, thu được các mô hình không thể chứng minh chính xác cấu trúc cơ bản của tập dữ liệu, do đó cũng thu được các tính năng của mô hình dự đoán không tốt.
Mặt khác, sai lệch phổ xảy ra khi tập dữ liệu được sử dụng để phát triển mô hình không đại diện cho dân số mục tiêu. Để tránh đánh giá quá cao độ chính xác và tổng quát, cần đảm bảo một tập dữ liệu xác nhận bên ngoài được thu thập theo cách giảm thiểu sai lệch phổ. Bên cạnh đó, các nghiên cứu quan sát đa trung tâm được thiết kế tốt là cần thiết để xác nhận rõ ràng hơn. Chắc chắn, cũng cần phải thừa nhận các vấn đề đạo đức vì AI không nhận thức được các lựa chọn hoặc trách nhiệm pháp lý của bệnh nhân. Các vấn đề về quyền riêng tư có thể được giải quyết bằng cách sử dụng các bộ dữ liệu được liên kết không liên quan đến các máy chủ tập trung. Các nghiên cứu ngẫu nhiên trong tương lai có thể trực tiếp làm tăng giá trị tổng thể (chất lượng so với chi phí) của CNN bằng cách kiểm tra tác động của nó đối với nội soi đại tràng giám sát, thời gian nội soi, polyp và ADR, và chi phí bệnh lý. Vì khoa học AI đang trong quá trình phát triển, những hạn chế hiện tại phải được coi là thách thức trong tương lai, vì vậy chúng thực sự được kế thừa trong các ứng dụng y học, bao gồm khả năng dự đoán khó đối với các tình huống có đặc điểm là không chắc chắn. Nhìn chung, AI đang cách mạng hóa công nghệ và tác động đến các khía cạnh đạo đức khác như thay thế công việc của con người bằng máy móc, nhưng đây luôn là một câu hỏi mở kể từ cuộc cách mạng công nghiệp. Điều có thể làm là thúc đẩy sự hợp tác lẫn nhau thông qua các ứng dụng nội soi tiêu hóa, để cùng hưởng lợi từ những thành tựu trong cả hai lĩnh vực khoa học.
Để chủ động bảo vệ sức khỏe, những đối tượng trên 40 tuổi, có tiền sử viêm teo dạ dày, viêm dạ dày mạn tính; Barrett thực quản; khối u dưới niêm mạc cần soi định kỳ kiểm tra; người bị thiếu máu không rõ nguyên nhân, sau cắt dạ dày, tiền sử gia đình có người mắc ung thư dạ dày nên tầm soát ung thư tiêu hóa đình kỳ. Hiện nay, Vinmec cung cấp Gói tầm soát và phát hiện sớm ung thư đường tiêu hóa (thực quản - dạ dày - đại tràng) kết hợp khám lâm sàng và cận lâm sàng để đem lại kết quả chính xác nhất có thể. Với gói khám này, bạn sẽ được:
- Khám Chuyên khoa Nội tiêu hóa;
- Nội soi dạ dày và nội soi đại tràng với máy nội soi NBI có gây mê;
- Nội soi dạ dày và nội soi đại tràng có gây mê;
- Xét nghiệm mô bệnh học thường quy cố định, chuyển, đúc, cắt, nhuộm...các bệnh phẩm sinh thiết (ống tiêu hóa trên (thực quản, dạ dày, tá tràng, papilla) qua nội soi;
- Xét nghiệm mô bệnh học thường quy cố định, chuyển, đúc, cắt, nhuộm...các bệnh phẩm sinh thiết (ống tiêu hóa dưới qua nội soi (đại tràng, trực tràng).
Nếu có nhu cầu khám và sử dụng các gói dịch vụ tại Vinmec, bạn hãy đăng ký đặt lịch ngay tại website hoặc liên hệ đến hệ thống hotline của Vinmec để được tư vấn chi tiết.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo
- Russell S, Norvig P. Artificial Intelligence: A Modern Approach, Global Edition. 3rd editon. London: Pearson, 2016.
- Colom R, Karama S, Jung RE, Haier RJ. Human intelligence and brain networks. Dialogues Clin Neurosci. 2010;12:489-501. [PubMed]
- Goodfellow I, Bengio Y, Courville A. Deep Learning. Cambridge: The MIT Press, 2016.
- Pohl H, Welch HG. The role of overdiagnosis and reclassification in the marked increase of esophageal adenocarcinoma incidence. J Natl Cancer Inst. 2005;97:142-146. [PubMed] [DOI]
- Dent J. Barrett's esophagus: A historical perspective, an update on core practicalities and predictions on future evolutions of management. J Gastroenterol Hepatol. 2011;26 Suppl 1:11-30. [PubMed] [DOI]
- Gaetano Cristian Morreale, Emanuele Sinagra, và cộng sự, Emerging artificial intelligence applications in gastroenterology: A review of the literature, Artif Intell Gastrointest Endosc. Jul 28, 2020; 1(1): 6-18