Bài viết bởi Tiến sĩ Thân Thị Trang Uyên - Chuyên viên Y tế - tế bào gốc - Viện nghiên cứu Tế bào gốc và Công nghệ gen Vinmec
Thể tiết ngoại bào là các túi kín nhỏ có kích thước nano và được tiết ra bởi nhiều loại tế bào khác nhau. Gần đây, ngày càng có nhiều báo cáo cho rằng thể tiết ngoại bào tiết ra từ tế bào gốc ung thư góp phần đáng kể vào sự tiến triển của khối u. Thực tế là do các EV này có liên quan đến các quá trình ức chế phát triển của khối u, di căn, hình thành mạch, cũng như duy trì kiểu hình gốc và vi môi trường ức chế miễn dịch khối u.
1. Giới thiệu tổng quan
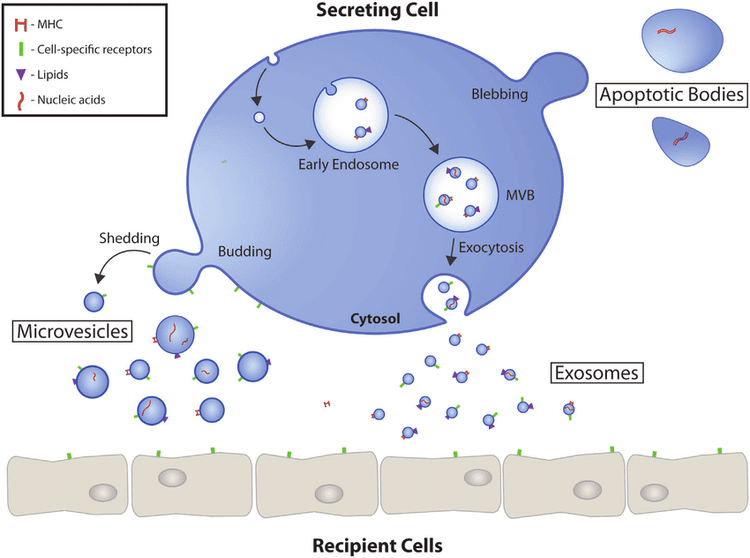
Thể tiết ngoại bào (extracellular vesicles - EV) là các túi kín nhỏ có kích thước nano và được tiết ra bởi nhiều loại tế bào khác nhau. Chúng được tìm thấy trong dịch cơ thể như huyết tương, dịch vết thương, nước tiểu, sữa mẹ ... và trong cả dịch nuôi cấy tế bào trong phòng thí nghiệm. EV có khả năng vận chuyển một số vật chất nhất định, chẳng hạn như axit nucleic, protein và lipid và được công nhận là chất trung gian quan trọng trong giao tiếp giữa tế bào với tế bào.
Tế bào gốc ung thư là gì? (Cancer stem cells - CSC). Thực tế, đây là một quần thể con của tế bào ung thư, có khả năng tăng sinh, tự tái tạo và biệt hóa. Sự hiện diện của CSC là nguyên nhân chính dẫn đến sự tiến triển và di căn của khối u. Gần đây, ngày càng có nhiều báo cáo cho rằng EV tiết ra từ CSC góp phần đáng kể vào sự tiến triển của khối u. Thực tế là do các EV này có liên quan đến các quá trình ức chế phát triển của khối u, di căn, hình thành mạch, cũng như duy trì kiểu hình gốc và vi môi trường ức chế miễn dịch khối u.
Là một nhóm không đồng nhất quan trọng trong các mô ung thư, CSC tiết ra các EV thực hiện nhiều chức năng sinh học, bao gồm cả việc thúc đẩy các đặc tính tế bào gốc của những tế bào không thuộc nhóm CSCs, kháng hóa trị liệu, di căn, hình thành mạch và ức chế miễn dịch. Hiểu được cơ chế giao tiếp tế bào trong môi trường hình thành khối u trung gian thông qua EVs như vậy sẽ giúp ích cho việc điều trị trúng đích CSC. So với EV tiết ra từ tế bào không phải là CSC thì EVs có nguồn gốc từ CSCs chứa nhiều chỉ thị tính gốc và protein tính gốc hơn, chẳng hạn như CD133, CD44, Notch1. Theo đó, các protein này trong EV sẽ được vận chuyển tới những tế bào không phải CSC để tăng cường tính gốc của chúng. Bên cạnh đó, EV có nguồn gốc từ CSC tạo ra tính không đồng nhất khối u tĩnh hoặc động ở vùng lân cận khối. CSC tiết ra EV vận chuyển các protein đặc hiệu và các yếu tố phiên mã đến các tế bào lân cận có tác động lớn hơn đến việc duy trì tính không đồng nhất của khối u.
Do vậy, hiểu được vai trò sinh học và cơ chế phân tử mà EV có nguồn gốc từ CSC trong sự tiến triển của khối u chắc chắn sẽ cung cấp những ý tưởng mới cho các chiến lược điều trị ung thư dựa trên tế thể tiết ngoại bào và tế bào gốc ung thư.
2. EV từ tế bào gốc ung thư cảm ứng dịch chuyển thành tế bào ung thư
Các EV tích cực tham gia vào các tương tác giữa tế bào với tế bào bằng cách vô hiệu hoặc kích hoạt các thành phần của tế bào đích. Các bằng chứng cho thấy rằng EV có nguồn gốc từ tế bào gốc ung thư (Cancer stem cells – CSC) đã thúc đẩy dịch chuyển các tế bào không phải CSC đạt được các đặc tính tế bào gốc, dẫn đến tăng cường khả năng sinh khối u.
Các nghiên cứu đã phát hiện ra rằng các EV tiết ra từ CSCs mang các chỉ thị tính gốc (stemness markers) của tế bào mẹ, có khả năng tái lập trình các tế bào không phải CSC để đạt được kiểu hình giống tế bào gốc. Ví dụ: CD44v6 và Tspan8, hai chỉ thị (marker) của tế bào khởi phát ung thư tuyến tụy (PaCIC), đã được phát hiện trong các EV có nguồn gốc từ PaCIC. Các EV chứa CD44v6 và Tspan8 có nguồn gốc từ PaCIC đã thúc đẩy tế bào không phải là PaCIC (đã được loại bỏ gen CD44v6 và Tspan8) chuyển hướng sang biểu hiện các đặc tính tế bào gốc ung thư. CD44v6 và Tspan8 từ EV hoạt động như một nhóm, được kích hoạt bởi RTK phụ thuộc vào CD44v6, GPCR và integrin.
Ngoài ra, nó cũng ảnh hưởng đến quá trình xử lý miRNA ở những tế bào không phải PaCIC. Do đó, một phương pháp điều trị đầy hứa hẹn cho ung thư tuyến tụy là ngăn chặn đặc hiệu sự tương tác giữa PaCIC-EV và những tế bào không phải PaCIC, chẳng hạn như việc sử dụng các chất ức chế RTK để chặn tín hiệu và kháng -Tspan8 để ngăn chặn sự hấp thu EV.
Ngoài các protein liên quan đến chỉ thị tính gốc, các nghiên cứu cũng phát hiện ra rằng CSCs-EV cũng chứa các protein liên quan đến việc kích hoạt các đường truyền tín hiệu tính gốc khối u. Chúng có thể trực tiếp kích hoạt các con đường tín hiệu liên quan đến tính gốc (stemness-related signaling pathway) của các tế bào không phải CSCs. Do đó, tạo điều kiện thuận lợi cho dịch chuyển sang kiểu hình tế bào gốc của chúng. Sự gia tăng biểu hiện protein Notch1 trong các EV có nguồn gốc từ tế bào gốc u nguyên bào thần kinh đệm (GSC) cũng sẽ kích hoạt hoạt động con đường tín hiệu Notch trong CSCs một cách bất thường. Notch1 từ EV có nguồn gốc GSCs đã tái lập trình các tế bào không phải GSC thành GSC và tăng cường đáng kể khả năng sinh khối u của chúng. Sau khi được điều trị bằng RNA can thiệp vào biểu hiện Notch1 hoặc điều trị bằng các yếu tố ức chế Notch, các tế bào không phải GSC được xử lý với GSC-EV giảm khả năng hình thành khối u cầu và giảm biểu hiện các protein mang tính gốc.

Ngoài ra, các EV có nguồn gốc từ CSC chứa lượng lớn RNA có thể tái lập trình các tế bào không phải CSC thành CSC bằng cách kích hoạt một số con đường liên quan đến tính gốc khác. Các EV được tiết ra bởi tế bào đại trực tràng biểu hiện marker CD133 vận chuyển cicrRNA-ABCC1 đến các tế bào CSC không thuộc đại trực tràng và thúc đẩy các tế bào này dịch chuyển sang biểu hiện kiểu hình gốc và khả năng hình thành khối u cầu. Về mặt cơ chế, EV cicRNA-ABCC1 kích hoạt con đường Wnt/β-catenin giúp thúc đẩy sự tiến triển của ung thư đại trực tràng. Hơn nữa, lncRNA FMR1-AS1 EV có nguồn gốc từ tế bào gốc ung thư nội mô đã truyền các đặc điểm giống gốc sang tế bào không phải CSCs trong môi trường khối u. lncRNA FMR1-AS1 trong EV liên kết với thụ thể giống Toll 7 (TLR7) nội bào và sau đó kích hoạt tín hiệu TLR7/NF-κB để thúc đẩy sự biểu hiện c-Myc. Do đó, kích thích sự tăng sinh tế bào gốc ung thư nội mô, chống chết theo chu trình apoptosis và tăng khả năng xâm nhập.
Do vậy, các EV từ CSC là nguồn mang vật chất sinh học có thể truyền tín hiệu kích thích chuyển đổi tế bào sang dạng ung thư và hình thành khối u. Dựa vào cơ chế này, có thể thiết kế EV là nguồn mang thuốc ức chế tế bào gốc ung thư nhằm đặc trị cho các khối u đích.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo:
Su, C., Zhang, J., Yarden, Y. et al. The key roles of cancer stem cell-derived extracellular vesicles. Sig Transduct Target Ther 6, 109 (2021). https://doi.org/10.1038/s41392-021-00499-2.