Bài viết được viết bởi Thạc sĩ, Bác sĩ Mai Viễn Phương- Bác sĩ nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
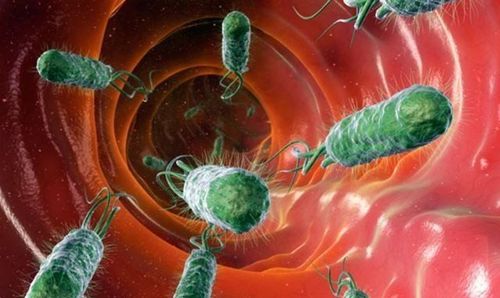
H. pylori là một vi khuẩn hình xoắn ốc sống trong lớp niêm mạc lót mặt trong dạ dày con người. Đây là loại vi khuẩn có liên quan trực tiếp đến bệnh ung thư dạ dày. Hiện tại tỷ lệ nhiễm vi khuẩn H. pylori được ghi nhận ở nước ta và trên thế giới với tỷ lệ khá cao.
1. Đặc tính sinh học của vi khuẩn H.Pylori
H. pylori là một vi khuẩn hình xoắn ốc sống trong lớp niêm mạc lót mặt trong dạ dày người. Sống trong môi trường acid khắc nghiệt của dạ dày. H. pylori tiết ra một enzym là urease làm chuyển đổi urea thành ammonium. Sự sản xuất ra ammonium quanh H.pylori làm trung hòa độ acid của dạ dày, làm cho vi khuẩn dễ sống hơn. Hơn nữa, hình xoắn ốc của H. pylori giúp nó đào bới vào trong lớp nhầy có độ acid kém hơn của thành dạ dày. H. pylori cũng có thể gắn vào các tế bào niêm mạc của dạ dày. Mặc dù, các tế bào miễn dịch bình thường nhận biết và tấn công vi khuẩn xâm nhập tập trung gần các vị trí nhiễm H. pylori, chúng vẫn không thể đi tới lớp niêm mạc dạ dày. Ngoài ra, H. pylori có nhiều cách cản trở các đáp ứng miễn dịch tại chỗ nên không thể thải trừ loại vi khuẩn này được.
H. pylori đã cùng tồn tại với con người trong hàng ngàn năm và sự nhiễm khuẩn với loại vi khuẩn này là rất phổ biến. Đánh giá của Trung tâm Kiểm soát và Phòng bệnh Hoa kỳ (CDC) có khoảng 2/3 dân số thế giới có loại vi khuẩn này ẩn náu, với tỷ lệ nhiễm cao hơn nhiều ở các nước đang phát triển so với các nước đã phát triển.
Mặc dù, nhiễm H. pylori không gây bệnh cho đa số người bị nhiễm, nó là một yếu tố nguy cơ lớn cho bệnh viêm loét dạ dày và chịu trách nhiệm về đa số các ổ loét ở dạ dày và đoạn trên của ruột non.
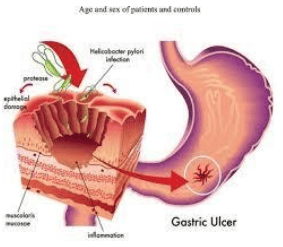
Nhiễm H. pylori là một yếu tố nguy cơ mạnh và đã được biết rõ của bệnh ung thư dạ dày được Cơ quan Nghiên cứu Ung thư Quốc tế (IARC) xếp loại là tác nhân gây ung thư nhóm 1. Đã có một số cơ chế bệnh sinh được đề xuất để giải thích vì sao nhiễm H. pylori có thể làm tăng nguy cơ ung thư dạ dày, nhưng phần lớn các tác giả đều cho rằng tình trạng viêm mạn tính lâu ngày là cơ chế chính.
H. pylori được cho là lan truyền qua thức ăn và nước uống bị nhiễm, qua tiếp xúc trực tiếp từ miệng tới miệng. Ở đa số dân, nhiễm vi khuẩn trước tiên là ở trẻ con, nhất là ở các xứ nghèo, nơi ở chật chội và kém vệ sinh.
2. Tỷ lệ nhiễm H. pylori ở Việt Nam hiện nay như thế nào?
Tại Việt Nam, tỷ lệ nhiễm H.pylori trong dân số khoảng 80%. Theo các báo cáo từ năm 2002 – 2006, tỷ lệ nhiễm H. pylori ở trẻ em là khá cao, từ 78,7% – 85,7%. Một nghiên cứu mới đây tại khoa Tiêu hóa – Bệnh viện Nhi đồng 1 thành phố Hồ Chí Minh, năm 2015, tỷ lệ nhiễm H.pylori xác định qua nội soi và làm mô bệnh học là 67,1% cho trẻ từ 15 tuổi trở xuống. Khoảng 20 năm qua trên thế giới đã có nhiều công bố và cảnh báo về nhiễm H. pylori trong cùng gia đình, đặc biệt là chính cha mẹ hoặc ông bà là nguyên nhân chủ yếu lây truyền bệnh cho trẻ. Tỷ lệ nhiễm H. pylori trong các biến chứng thủng do loét dạ dày-tá tràng ở Việt Nam và trên thế giới vào khoảng 80-100%. Trong biến chứng chảy máu do loét dạ dày-tá tràng, tỷ lệ này khoảng 60-85%. Trong bệnh ung thư dạ dày, tỷ lệ nhiễm H.pylori khoảng 80% trường hợp.
3. Ung thư dạ dày là gì và có triệu chứng như thế nào?
Ung thư dạ dày trước đây được coi là một thực thể duy nhất. Nay các nhà khoa học chia ra làm hai lớp chính: ung thư tâm vị dạ dày (ung thư của in-sơ đầu tiên của dạ dày, nơi tiếp nối với thực quản) và ung thư dạ dày không phải tâm vị (ung thư ở tất cả các vùng còn lại của dạ dày). Nhiễm H. pylori là nguyên nhân đầu tiên được xác định của ung thư dạ dày. Các yếu tố nguy cơ khác bao gồm: viêm dạ dày mạn tính, tuổi già, nam giới; ăn nhiều muối, hút thuốc, dùng thức ăn bảo quản kém, ăn ít hoa quả và rau cỏ, bệnh thiếu máu ác tính, đã có tiền sử mổ dạ dày trước đó vì các bệnh lành tính, trong gia đình có người bị ung thư dạ dày.
Tỷ lệ kết hợp của H. pylori với hai lớp chính của ung thư dạ dày không giống nhau. Trong khi người nhiễm H. pylori có nguy cơ gia tăng với ung thư dạ dày không phải tâm vị, các nguy cơ của ung thư tâm vị lại không tăng và còn có thể sụt giảm.

4. Triệu chứng bệnh dạ dày do nhiễm vi khuẩn H.pylori như thế nào?
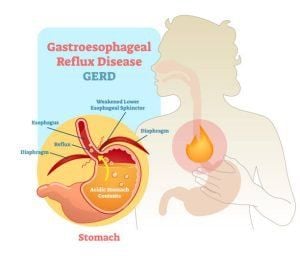
Khi bị nhiễm H. pylori gây ra bệnh viêm, loét và có thể cả ung thư dạ dày, người bệnh có các biểu hiện khác nhau như: ăn vào có cảm giác nóng bụng, đầy hơi, khó tiêu, ợ hơi, cảm giác khó thở (khám tim mạch và hô hấp bình thường). Người bệnh có các rối loạn tiêu hóa khác như đi tiêu phân sống, tiêu chảy, có thể tê chân tay, đau đầu, hơi thở có mùi hôi đặc trưng. Khi kèm theo triệu chứng trào ngược dịch vị từ dạ dày lên miệng, người bệnh có thể bị viêm họng do trào ngược, sâu răng...
5. H. pylori cagA dương tính là gì và chúng có ảnh hưởng thế nào đến nguy cơ ung thư dạ dày, thực quản?
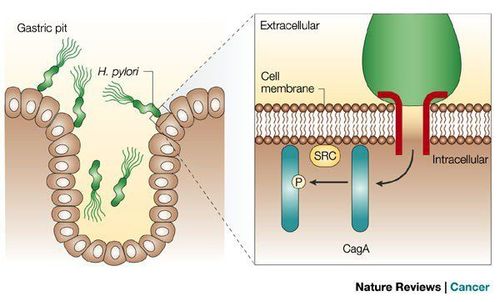
Một số ít vi khuẩn H. pylori sử dụng một phần phụ giống cái kim để tiêm một độc tố sản xuất do một gen có tên là cagA (gen A kết hợp với độc tố tế bào / cytotoxin-associated gen A) vào các đoạn nối giữa các tế bào lót dạ dày. Độc tố cagA làm biến đổi cấu trúc các tế bào dạ dày và làm cho vi khuẩn gắn vào chúng dễ dàng hơn. Sự phơi bày lâu dài với độc tố gây ra viêm mạn tính. Khoảng 60% H. pylori ở các nước phương Tây và hầu hết H. pylori ở các nước Đông Á có cagA-dương tính. Bằng chứng dịch tễ học đưa ra giả thuyết là nhiễm giống cagA-dương tính đặc biệt kết hợp với tăng nguy cơ ung thư dạ dày không phải tâm vị và giảm các nguy cơ của ung thư dạ dày tâm vị cũng như ung thư biểu mô tuyến thực quản. Ví dụ, một phân tích tổng hợp của 16 nghiên cứu kiểm tra bệnh chứng tiến hành trên thế giới cho thấy những người nhiễm H.pylori cagA-dương tính có nguy cơ ung thư dạ dày không phải tâm vị cao gấp đôi so với những người nhiễm H. pylori cagA-âm tính.
Ngược lại, một nghiên cứu bệnh chứng tiến hành ở Thụy Điển cho thấy người bị nhiễm H.pylori cagA-dương tính có nguy cơ ung thư biểu mô tuyến thực quản giảm có ý nghĩa thống kê. Tương tự, một nghiên cứu bệnh chứng khác ở Hoa Kỳ cho thấy nhiễm H. pylori cagA-dương tính kết hợp với giảm nguy cơ ung thư biểu mô tuyến thực quản và ung thư dạ dày tâm vị phối hợp, nhưng nhiễm các chủng cagA- âm tính thì không có nguy cơ. Một nghiên cứu gần đây đã gợi ý một cơ chế có khả năng mà theo đó CagA có thể tham gia vào quá trình sinh ung thư biểu mô của dạ dày. Trong ba nghiên cứu, nhiễm H. pylori với CagA-dương tính kết hợp với sự bất hoạt của các protein triệt u, kể cả p53.
H. pylori có khả năng thích nghi đặc biệt để sống trong môi trường acid thù địch ở dạ dày và sự trú đóng của H. pylori gây nên viêm dạ dày ở hầu hết số đối tượng bị nhiễm vi khuẩn này. Sự bám dính của vi khuẩn vào tế bào biểu mô gây nên một đáp ứng viêm, với sự tập trung của bạch cầu trung tính rồi sau đó là các tế bào lympho B và T, đại thực bào và tương bào, phần lớn đều sản sinh một lượng lớn các nhóm oxy hoặc nitơ phản ứng những gốc tự do gây hư tổn tế bào biểu mô và sinh ung thư.
Sự hư tổn niêm mạc dạ dày do nhiễm H. pylori còn có thể vì các yếu tố độc lực của vi khuẩn được mã hóa bởi “cag pathogenicity island” [Tên gọi đầy đủ là cytotoxin-associated gene pathogenicity island (cag-PAI), một hệ thống phân tiết týp IV (T4SS) đặc biệt, được mã hóa bởi các chủng Helicobacter pylori týp 1. T4SS được vi khuẩn sử dụng để trao đổi chất, ADN hoặc protein với môi trường bên ngoài (ND).], như cyto-toxin A tạo không bào (VacA) và protein CagA (CagA). VacA là một toxin được vi khuẩn tiết ra và đi vào màng tế bào biểu mô, tạo không bào và ảnh hưởng các ti thể, dẫn đến vong bào (apoptosis) [Galmiche A và cs, 2000; Kuck D và cs, 2001]. Trái lại, CagA khi vào trong tế bào biểu mô lại gây phát tín hiệu tăng sinh và vận động, cũng như sản xuất các cytokine [Keates S, và CS. 1999]. CagA gây nên sự biến đổi hình thái tế bào ký chủ qua cơ chế tương tác với protein SHP-2, một tyrosin phosphatase trong bào tương [Higashi H và cs, 2002]. Thật vậy, sau khi vào trong tế bào, trước tiên CagA được tyrosin-phosphoryl hóa bởi họ kinase Src, rồi sau đó gắn với SHP-2. Vì SHP-2 có vai trò quan trọng trong các hiện tượng tải nạp (transduction) do nhiều thụ thể tyrosin kinase khác nhau thực hiện, nên CagA gây rối loạn chức năng tế bào bằng cách làm mất chức năng điều hòa của SHP-2, ức chế sự tái phối trí khung tế bào, sự tăng sinh và làm tăng chuyển động trong tế bào biểu mô dạ dày.
Ngoài ra, có giả thiết cho rằng tính đa hình của cag, vốn nằm trong chuỗi mã hóa gốc tyrosin, có thể là những biến số thiết yếu của kết cục lâm sàng khi bị nhiễm bởi các chủng H. pylori cag+ khác nhau. Thật vậy, H. pylori có thể chia thành hai phân nhóm chính dựa trên sự tyrosin-phosphoryl hóa/vị tri gắn SHP-2 khác nhau về mặt cấu trúc: chủng cag+ Đông Á và chủng cag+ phương Tây. Cụ thể, bệnh nhân bị nhiễm chủng Đông Á có tăng đáp ứng viêm, tổn thương tiền ung thư dạ dày ở mức cao hơn và có nguy cơ ung thư dạ dày lớn hơn so với bệnh nhân nhiễm các chủng vi khuẩn phương Tây.
Hơn nữa, nhiễm H. pylori cag+ làm tăng biểu hiện COX-2 ở niêm mạc dạ dày và ung thư [Guo XL và cs, 2003]. COX-2 thường không phát hiện được trong mô bình thường và trở nên phong phú ở nơi bị viêm và cũng có thể biểu hiện thái quá trong ung thư dạ dày. Sự biểu hiện thái quá của COX-2 dẫn đến tăng tổng hợp và phóng thích prostaglandin, như PGE2 chẳng hạn. Sự gia tăng prostaglandin này thúc đẩy quá trình sinh ung thư bằng cách đẩy mạnh tăng sinh tế bào, ức chế vong bào và làm tăng tính xâm lấn của tế bào ác tính [Yamac D và cs, 2008]. Sự biểu hiện COX-2 giảm đáng kể sau khi tiệt trừ H. pylori trên bệnh nhân viêm teo dạ dày, khẳng định vai trò then chốt của vi khuẩn trong cơ chế bệnh sinh qua COX-2 [Konturek PC và cs, 2003].
Ngày càng có nhiều bằng chứng khẳng định tầm quan trọng của sự biến thiên di truyền trong cơ chế bệnh sinh của ung thư dạ dày và những tổn thương tiền ung thư. Tính đa dạng cơ năng của TLR4, một thụ thể lipopolysaccharide (LPS) trên bề mặt tế bào tham gia vào sự nhận biết H. pylori và đáp ứng của ký chủ, có sự kết hợp với tăng mức độ viêm với sự hư tổn mô nặng trên người bị nhiễm H. pylori. Cụ thể, người mang tính đa dạng TLR4+896A>G có nhiều khả năng teo dạ dày và viêm nặng hơn và cũng tăng nguy cơ ung thư dạ dày ngoài tâm.
Sau cùng, tính đa dạng và độ biến thiên di truyền của các yếu tố bệnh sinh thiết yếu như các gen cagA, TRL4 và SHP2 tỏ ra ảnh hưởng đến tiềm năng sinh ung thư của các chủng H. pylori. Do đó, điều quan trọng là nhận ra và phân biệt các chủng H. pylori hay gây ung thư và nhận diện những quần thể nguy cơ cao về mặt di truyền dễ mắc ung thư dạ dày.
Tuy có nhiều cơ chế phân tử khẳng định vai trò của H. pylori trong ung thư dạ dày, nhưng nhiễm H. pylori không được xem là “điều kiện đủ” để phát bệnh ung thư [Fock KM và cs, 2008]. Thật vậy, chỉ một thiểu số đối tượng nhiễm vi khuẩn bị ung thư dạ dày, vì có nhiều yếu tố ký chủ và môi trường tác động hiệp lực trong căn bệnh đa yếu tố này.
Vi khuẩn H. pylori là loại vi khuẩn có những đặc điểm khác biệt với nhiều loại vi khuẩn khác, một trong các yếu tố cơ bản giúp H. pylori có thể tồn tại lâu dài trong môi trường axit dạ dày là vi khuẩn H. pylori có thể tiết ra men urease, và urease có khả năng trung hòa axit giúp tạo nên môi trường phù hợp để vi khuẩn H. pylori không bị axit dạ dày tiêu diệt.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.